Giải bài tập Hóa 10 Bài 6: Luyện tập: Cấu tạo vỏ nguyên tử
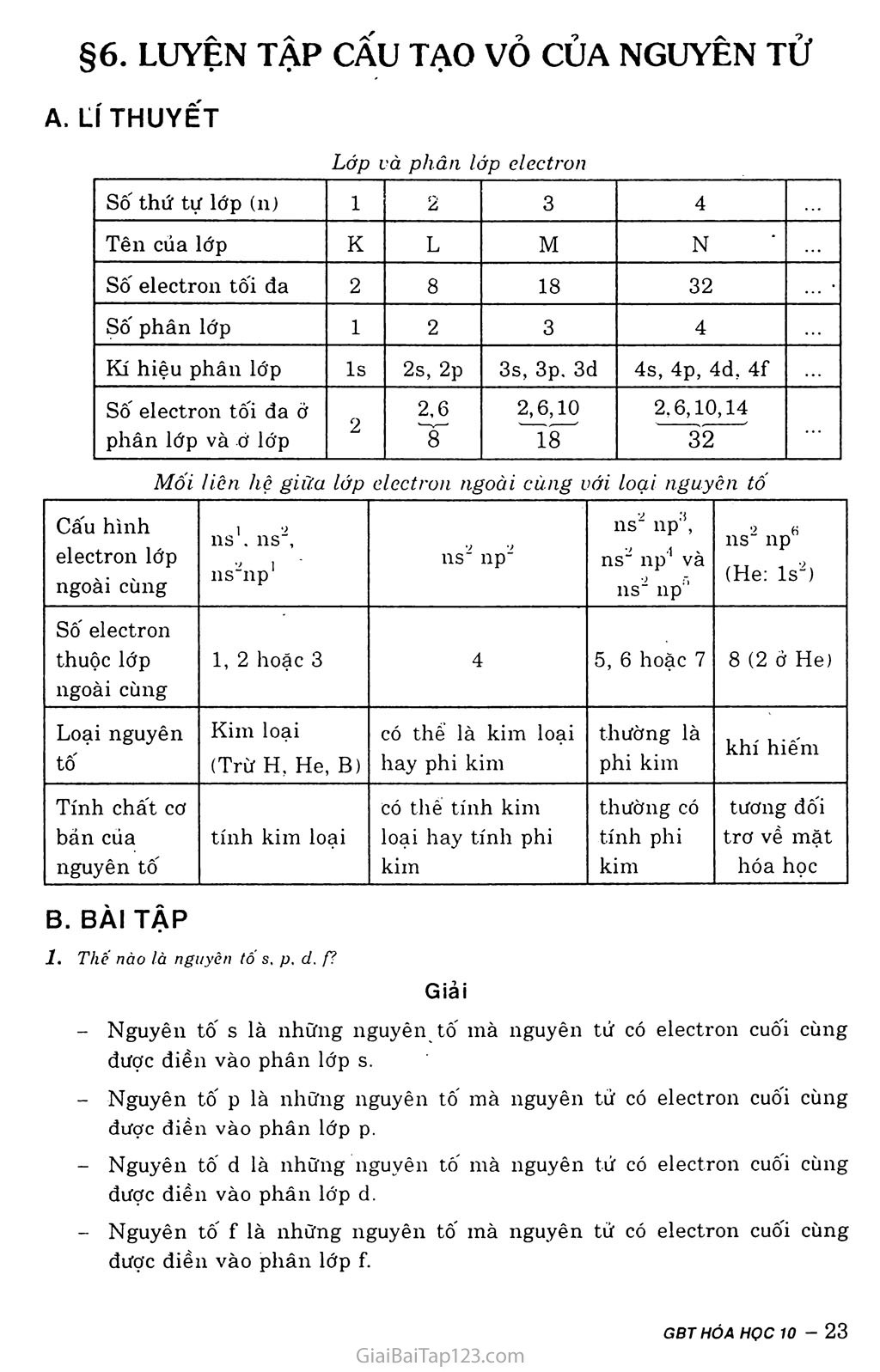
§6. LUYỆN TẬP CẤU TẠO vỏ CỦA NGUYÊN TỬ A, Lí THUYẾT Lớp và phân lớp electron Sô' thứ tự lớp (n) 1 2 3 4 Tên của lớp K L M N Số electron tối đa 2 8 18 32 Sô' phân lớp 1 2 3 4 Kí hiệu phân lớp ls 2s, 2p 3s, 3p, 3d 4s, 4p, 4đ, 4f Sô' electron tô'i đa ở phân lớp và ơ lớp 2 2,6 8 2,6,10 18 2.6,10,14 32 Mối liên hệ giữa lớp electron ngoài cùng với loại nguyên tố Câ'u hình electron lớp ngoài cùng ns1, ns', ns'np1 ns" np" ns2 np:i, ns' np’ và ns2 np’’ ns2 npK (He: ls2) Sô' electron thuộc lớp ngoài cùng 1, 2 hoặc 3 4 5, 6 hoặc 7 8 (2 ở He) Loại nguyên tố Kim loại (Trừ H, He, B) có thế là kim loại hay phi kim thường là phi kim khí hiếm Tính chất cơ bản của nguyên tô' tính kim loại có thê tính kim loại hay tính phi kim thường có tính phi kim tương đối trơ về mặt hóa học B. BÀI TẬP 1. Thế nào là nguyên tố s. p, d, f? Giải Nguyên tố s là những nguyên tố mà nguyên tứ có electron cuối cùng được điền vào phân lớp s. Nguyên tô p là những nguyên tô mà nguyên tử có electron cuối cùng được điền vào phân lớp p. Nguyên tố d là những nguyên tố mà nguyên tử có electron cuối cùng được điền vào phân lớp d. Nguyên tô' f là những nguyên tô' mà nguyên tử có electron cuối cùng được điền vào phân lớp f. Các electron thuộc tap K hay láp L liên két với hạt nhăn chặt chẽ hơn? Vi sao? Giải Các electron thuộc lớp K liên kết với hạt nhân chặt chẽ hơn các electron thuộc lớp L, vì gần hạt nhân hơn và mức năng lượng thấp hơn. Trong nguyên tứ, những electron cùa lớp nào quyết định tinh chốt hóa học của nguyên tử nguyên tố đó? Cho vi dụ. Giải Trong nguyên từ, những electron ở lớp ngoài cùng quyết định tính chất hóa học của nguyên từ nguyên tô' đó. Ví dụ: oxi có 6e, lưu huỳnh có 6e ở lớp ngoài cùng nên đều thế hiện tính chất phi kim. vỏ electron của một nguyên tử có 20 electron. Hỏi: Nguyên tử đó có bao nhiêu lớp electron? Lớp ngoài cùng có bao nhiêu electron? Nguyên tố dó là kim loại hay phi kim:? Giải Viết câ'u hình electron: ls22s22p63s23pB4s2. Nguyên tử đó có 4 lớp electron. Lớp ngoài cùng có 2 electron. Đó là kim loại. Cho biêt sô' electron tôi đa ớ các phàn lớp sau: 2s; b) 3p; c) 4s; d) 3d. Giải Phân lớp s chỉ có 1 obitan ( I I ) nên chứa tô'i đa 2 electron. Phân lớp p chỉ có 3 obitan ( i 1 I I) nên chứa tối đa 6 electron. Phân lớp d chỉ có 5 obitan ( 1- 1 1 I 3—1 ) nên chứa tô'i đa 10 electron. Đáp số: a) 2s2 b) 3pB c) 4s2 d) 3d10. Cấu hình electron ciia nguyên tử photpho tà ls22s22p63s23p3. Hỏi: Nguyên tứ photpho có bao nhiêu electron ? Sô hiệu nguyên tử của photpho là bao nhiêu? Lớp electron nào có mức nàng lượng cao nhất? Có bao nhiêu lớp electron, mồi lớp có bao nhiêu electron? Photpho là nguyên tố him loại hay phi kim? Vỉ sao? Giải Từ cấu hình electron của nguyên tử photpho, ta có: Nguyên tử photpho có 15 electron. Sô' hiệu nguyên tử của p là 15. Lớp thứ ba có mức năng lượng cao nhất. Có 3 lớp, cấu hình theo lớp: 2, 8, 5. Photpho là phi kim, vì có 5e ở lớp ngoài cùng. Cấu hình electron của nguyên từ cho ta biết những tliông tin gi? Cho ri dụ. Giải Người ta dùng câ'u hình electron nguyên tử đế biểu diễn sự phân bô' electron trên cùng các lớp và phân lớp. Từ đó dự đoán được nhiều tính chất của nguyên tử. Ví. dụ: Ar (ls22s22p63s23pti) là khí hiếm. Viết cấu hình electron đáy đủ cho các nguyên tử có lớp electron ngoài cùng là: a) 2s1; d)3s23p3; a) ls22s'; d) ls22s22pB3s23p3; 9. Cho biết tên, kí hiệu. sô hi.Ị 2 nguyên tố có số electro 2 nguyên tó co ĩ electron 2 nguyên tố có 7 electron 2s~2p3; ei 3s23p:’; Giải b) ls22s22p3; e) ls22s22pB3s23p5; u nguyên tử của: I lớp ngoài cùng là tói đa: ớ láp ngoài cùng: ó lớp ngoài cúng. 2s-2pG; g) 3s23p':. ls22s22pB; g) ls22s22pB3s23pB. Giải 2 nguyên tô' có số electron lớp ngoài cùng là tô'i đa là: “Ne, (Z = 10): ls22s22pri. '“’Ar , (Z = 18): ls22s22p63s23p6. 2 nguyên tô' có 1 electron ở lớp ngoài cùng là: “Na, (Z = 11): ls22s22p63sJ. “K , (Z = 19): ls22s22pB3s23pB4s'. 2 nguyên tô' có 7 electron ớ lớp ngoài cùng là: 'gF , (Z = 9): ls22s22p5. “Cl, (Z = 17): ls22s22pB3s23p5. Đáp số: a) “Ne ; “Ar b) “Na ; “K c) '°F ; “C1 .