SGK Hóa Học 8 - Bài 16: Phương trình hóa học
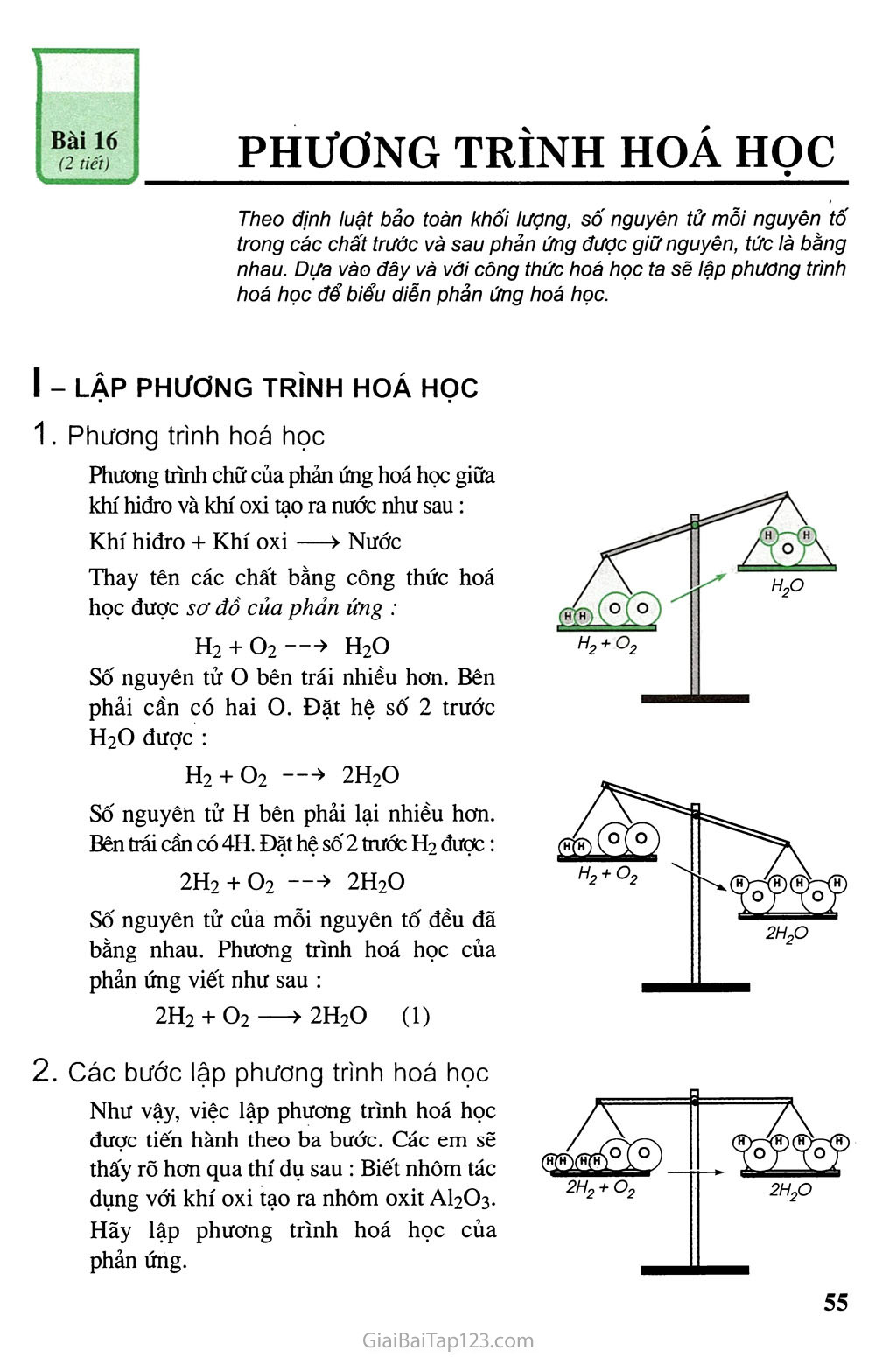
PHƯƠNG TRÌNH HOÁ HỌC Theo định luật bảo toàn khối lượng, số nguyên tử mỗi nguyên tố trong các chất trưởc và sau phản ứng được giữ nguyên, tức là bằng nhau. Dựa vào đây và với công thức hoá học ta sẽ lập phương trình hoá học để biểu diễn phản ứng hoá học. I - LẬP PHƯƠNG TRÌNH HOÁ HỌC Phương trình hoá học Phương trình chữ của phản ứng hoá học giữa khí hiđro và khí oxi tạo ra nước như sau : Khí hiđro + Khí oxi —> Nước Thay tên các chất bằng công thức hoá học được sơ đồ của phản ứng : H? + O2 H2O Số nguyên tử o bên trái nhiều hơn. Bên phải cần có hai o. Đặt hệ số 2 trước H2O được: H2 + O2 —* 2H2O Số nguyên tử H bên phải lại nhiều hơn. Bên trái cần có 4H. Đặt hệ số 2 trước H2 được: 2H2 + 02 —> 2H2O Số nguyên tử của mỗi nguyên tố đều đã bằng nhau. Phương trình hoá học của phản ứng viết như sau : 2H2 + O2—>2H2O (1) Các bước lập phương trình hoá học 2H2 + O2 2H2O Như vậy, việc lập phương trình hoá học được tiến hành theo ba bước. Các em sẽ thấy rõ hơn qua thí dụ sau : Biết nhôm tác dụng với khí oxi tạo ra nhôm oxit AI2O3. Hãy lập phương trình hoá học của phản ứng. Bước 1. Viết sơ đồ của phản ứng : AI + O2 AI2O3 Bước 2. Cân bằng số nguyên tử của mỗi nguyên tố : Số nguyên tử AI và o đều không bằng nhau, nhưng nguyên tố oxi có số nguyên tử nhiều hơn. Ta bắt đầu từ nguyên tố này. Trước hết làm chẵn số nguyên tử o ở bên phải, tức đặt hệ số 2 trước AI2O3, được : AI + O2 » 2AI2O3 Bên trái cần có 4A1 và 60 tức 3O2, các hệ số 4 và 3 là thích hợp. Bước 3. Viết phương trình hoá học : 4A1 + 3O2 —> 2AI2O3 (2) Lưu ý Không viết 60 trong phương trình hoá học, vì khí oxi ở dạng phân tử O2. Tức là không được thay đổi chỉ số ương những công thức hoá học đã viết đúng. Viết hệ số cao bằng kí hiệu, thí dụ không viết 4AI. Nếu trong công thức hoá học có nhóm nguyên tử, thí dụ nhóm (OH), nhóm (SO4)... thì coi cả nhóm như một đơn vị để cân bằng. Trước và sau phản ứng số nhóm nguyên tử phải bằng nhau(*\ Thí dụ, lập phương trình hoá học của phản ứng thực hiện trong bài 14, bài thực hành 3 (thí nghiệm 2.b). Phương trình chữ của phản ứng như sau : Natri cacbonat + Canxi hiđroxit —> Canxi cacbonat + Natri hiđroxit Viết sơ đồ của phản ứng : Na2CO3 + Ca(0H)2 —> CaCO3 + NaOH Số nguyên tử Na cũng như số nhóm (OH) ở bên trái đều là 2 và ở bên phải đều là 1. Còn số nguyên tử Ca và số nhóm (CO3) ở hai bên đều đã bằng nhau. Chỉ cần đặt một hệ số (hãy tự chọn) trước công thức một chất là viết được phương trình hoá học : Na2CO3 + Ca(0H)2 > CaCO3 + ?NaOH (3) Trừ nhưng phản ứng trong đó có nhóm nguyên tử không giư nguyên sau phản ứng. Khi đó phải tính số nguyên tử mỗi nguyên tố. II - Ý NGHĨA CỦA PHƯƠNG TRÌNH HOÁ HỌC Phương trình hoá học cho biết : Tỉ lệ về số nguyên tử, số phân tử giữa các chất trong phản ứng. Tỉ lệ này bằng đúng tỉ lệ hệ số mỗi chất trong phương trình. Thí dụ, theo phương trình hoá học (2) có tỉ lệ chung : Số nguyên tử AI : Số phân tử O2 : Số phân tử AI2O3 = 4:3:2 Hiểu là : cứ 4 nguyên tử AI tác dụng với 3 phân tử O2 tạo ra 2 phân tử AI2O3. Thường chỉ quan tâm đến tỉ lệ từng cặp chất, thí dụ : Cứ 4 nguyên tử AI tác dụng với 3 phân tử O2. Cứ 4 nguyên tử AI phản ứng tạo ra 2 phân tử AI9O3. Hay cứ 2 nguyên tử AI phản ứng tạo ra 1 phân tử AI2O3. Thử nghĩ xem còn có tỉ lệ của cặp chất nào nữa ? Phương trình hoá học biểu diễn ngắn gọn phản ứng hoá học. Ba bước lập phương trình hoá học : Viết sơ đồ của phản ứng, gồm công thức hoá học của các chất phản ứng và sản phẩm. Căn bằng sô' nguyên tủ mỗi nguyên tô': tìm hệ sô thích hợp đặt trước các công thức. — Viết phương trình hoá học. Phương trình hoá học cho biết tỉ lệ về số nguyên tử, sô phân tử giữa các chất cũng như từng cặp chất trong phản ứng. BÀI TẬP a) Phương trình hoá học biểu diễn gì, gồm công thức hoá học của những chất nào ? Sơ đổ của phản ứng khác với phương trình hoá học của phản ứng ở điểm nào ? Nêu ý nghĩa của phương trình hoá học. Cho sơ đồ của các phản ứng sau : Na + O2 > Na2Ũ P2O5 + H2O —> H3PO4 Lập phương trình hoá học và cho biết tỉ lệ số nguyên tử, số phân tử của các chất trong mỗi phản ứng. Yêu cầu làm như bài tập 2, theo sơ đồ của các phản ứng sau : HgO > Hg + O2 Fe(OH)3 —> Fe2O3 + H2O Cho sơ đồ của phản ứng sau : Na2CO3 + CaCI2 > CaCO3 + NaCI Lập phương trình hoá học của phản ứng. Cho biết tỉ lệ số phân tử của 4 cặp chất trong phản ứng (tuỳ chọn). Biết rằng kim loại magie Mg tác dụng với axit sunfuric H2SO4 tạo ra khí hiđro H2 và chất magie sunfat MgSO4. Lập phương trình hoá học của phản ứng. Cho biết tỉ lệ giữa số nguyên tử Mg lần lượt với số phân tử của ba chất khác trong phản ứng. Biết rằng photpho đỏ p tác dụng với khí oxi tạo ra hợp chất P2O5. Lập phương trình hoá học của phản ứng. Cho biết tỉ lệ giữa số nguyên tử p lần lượt với số phân tử của hai chất khác trong phản ứng. Hãy chọn hệ số và công thức hoá học thích hợp đặt vào những chỗ có dấu hỏi trong các phương trình hoá học sau (chép vào vở bài tập) : a) ?Cu + ? — -> 2CuO b) Zn + ?HCI -> ZnCI2 + H2 c) CaO + ?HNO3 — -> Ca(NO3)2 + ?