SGK Hóa Học 12 - Bài 33: Hợp kim của sắt
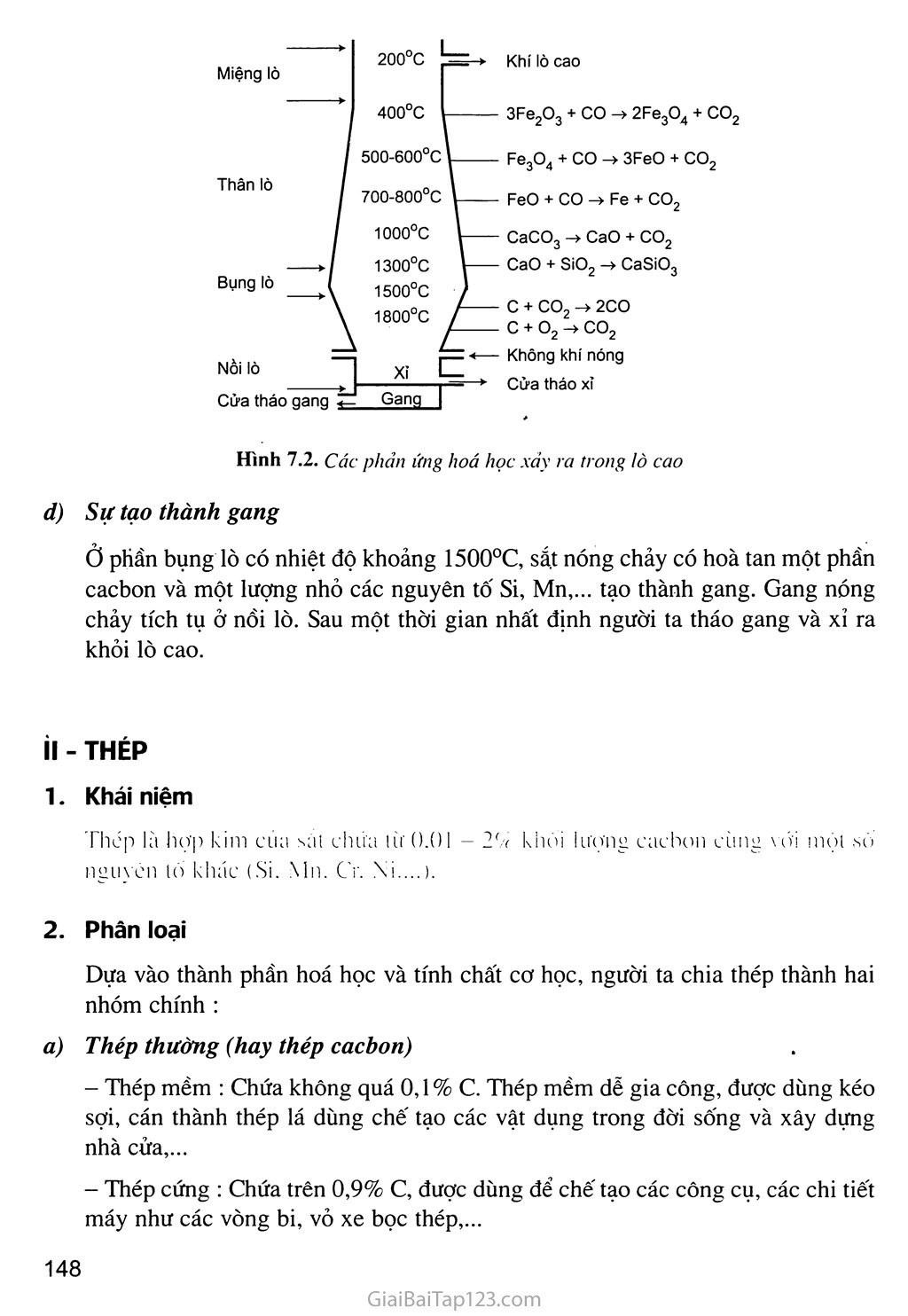
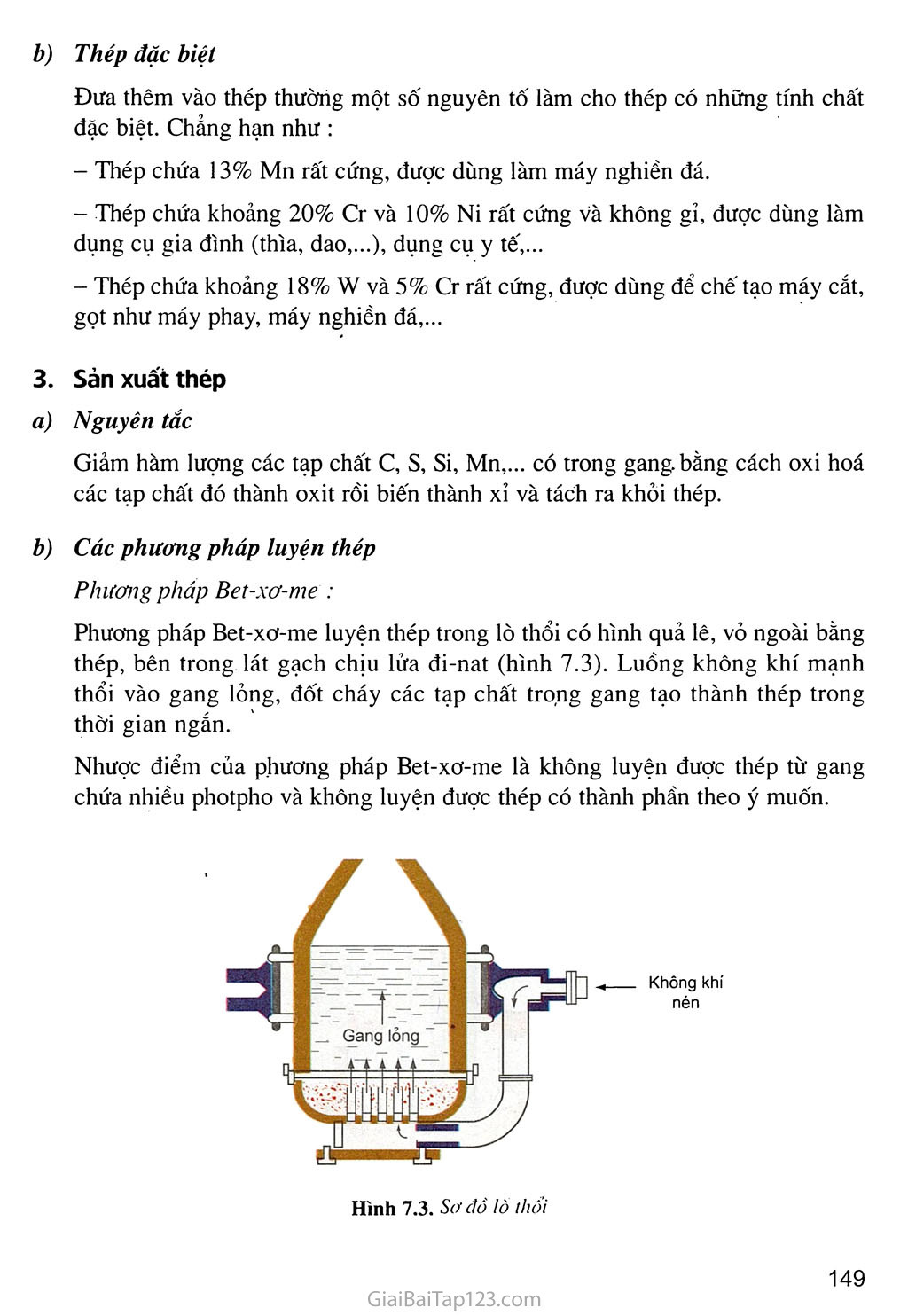
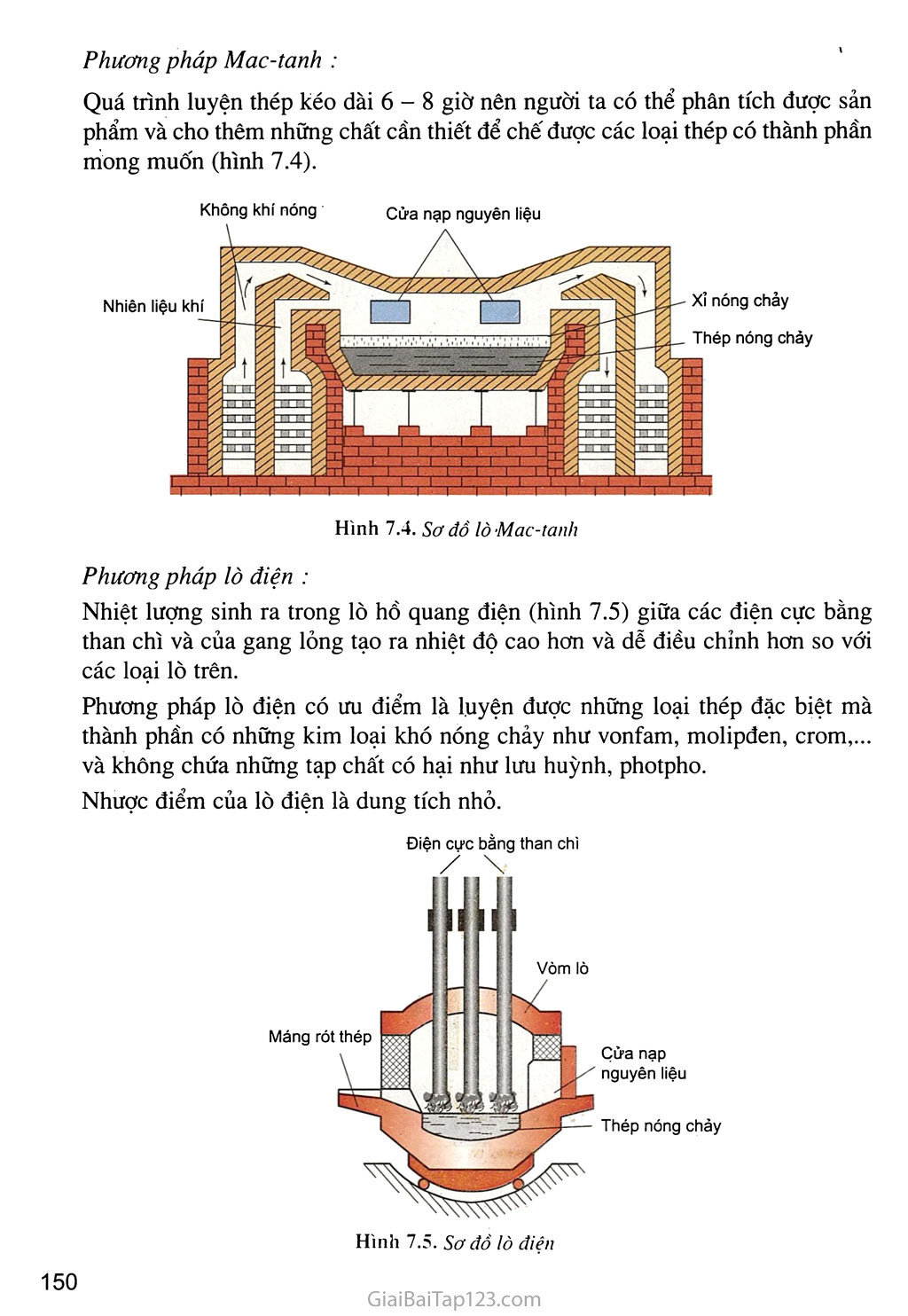
HỌP KIM CỦA SẮT Biết thành phần, tính chất và ứng dụng của gang, thép. Biết nguyên tắc và quy trình sản xuất gang, thép. I- GANG Khái niệm Gang là họ'p kim của sắt với cacbon trong đó có từ 2 - 5% khối lượng cacbon, ngoài ra còn một lượng nhỏ các nguyên tố Si, Mn, s,... Phân loại Có 2 loại gang Gang xám Gang chứa cacbon ở dạng than chì. Gang xám được dùng để đúc bệ máy, ống dẫn nước, cánh cửa,... Gang trắng Gang chứa ít cacbon hơn và cacbon chủ yếu ở dạng xementit (Fe3C). Gang trắng (có màu sáng hơn gang xám) được dùng để luyện thép. Sàn xuất gang Nguyên tắc Khử quặng sắt oxit bằng than cốc trong lò cao (hình 7.2). Nguyên liệu Quặng sắt oxit (thường là quặng hematit đỏ Fe2O3), than cốc và chất chảy (CaCO3 hoặc SiO2). ' . . Các phản ứng hoá học xảy ra trong quá trình luyện quặng thành gang • Phản ứng tạo thành chất khử co Không khí nóng được nén vào lò cao ở phần trên của nồi lò, đốt cháy hoàn toàn than cốc (hình 7.2). c + 02 —ĩì-> co2 Nhiệt lượng của phản ứng toả ra làm cho nhiệt độ lên tới trên 1800°C. Khí COọ đi lên phía trên, gặp lớp than cốc, bị khử thành co : co2 + c —2CO Phản ứng này thu nhiệt làm cho nhiệt độ phần trên của bụng lò vào khoảng 1300°C. • Phản ứng khử sắt oxit Các phản ứng co khử các sắt oxit đều được thực hiện trong phần thân lò, có nhiệt độ từ 400-800°C. Phần trên của thân lò có nhiệt độ khoảng 400°C xảy ra phản ứng : 3Fe2O3 + CO —2Fe3O4 + CO2t Phần giữa của thân lò có nhiệt độ khoảng 500-600°C xảy ra sự khử oxit sắt từ (Fe3O4) thành sắt(II) oxit (FeO) : Fe3O4 + CO —3FeO + CO2T Phần dưới của thân lò có nhiệt độ khoảng 700-800°C xảy ra phản ứng khử FeO thành Fe : FeO + CO —> Fe + CO2f Phản ứng tạo xỉ Ở phần bụng lò, nơi có nhiệt độ khoảng 1000°C xảy ra phản ứng phân huỷ CaCO3 và phản ứng tạo xỉ : CaCO3 -> CaO + CO2T CaO + SiOọ —> CaSiO3 (canxi silicat) Miệng lò Khí lò cao 3Fe2O3 + CO —> 2Fe3O4 + CO2 Fe3O4 + CO —> 3FeO + CO2 FeO + CO —> Fe + CO2 CaCO3 -> CaO + CO2 CaO + SiO2 -> CaSiO3 c + co2 -> 2CO c + 02 -+ co2 Không khí nóng Cửa tháo xì Hình 7.2. Các phản ứng hoá học xảy ra trong lò cao đ) Sự tạo thành gang ở phần bụng lò có nhiệt độ khoảng 1500°C, sắt nóng chảy có hoà tan một phần cacbon và một lượng nhỏ các nguyên tố Si, Mn,... tạo thành gang. Gang nóng chảy tích tụ ở nồi lò. Sau một thời gian nhất định người ta tháo gang và xỉ ra khỏi lò cao. II - THÉP Khái niệm Thép là hợp kim của sắt chứa từ 0,01 - 2% khối lượng cacbon cùng với một số nguyên tố khác (Si, Mn, Cr, Ni,...). Phân loại Dựa vào thành phần hoá học và tính chất cơ học, người ta chia thép thành hai nhóm chính : a) Thép thường (hay thép cacbon) Thép mềm : Chứa không quá 0,1% c. Thép mềm dễ gia công, được dùng kéo sợi, cán thành thép lá dùng chế tạo các vật dụng trong đời sống và xây dựng nhà cửa,... Thép cứng : Chứa trên 0,9% c, được dùng để chê' tạo các công cụ, các chi tiết máy như các vòng bi, vỏ xe bọc thép,... b) Thép đặc biệt Đưa thêm vào thép thường một số nguyên tố làm cho thép có những tính chất đặc biệt. Chẳng hạn như : Thép chứa 13% Mn rất cứng, được dùng làm máy nghiền đá. Thép chứa khoảng 20% Cr và 10% Ni rất cứng và không gỉ, được dùng làm dụng cụ gia đình (thìa, dao,...), dụng cụ y tế,... Thép chứa khoảng 18% w và 5% Cr rất cúng, được dùng để chế tạo máy cắt, gọt như máy phay, máy nghiền đá,... Sản xuất thép Nguyên tắc Giảm hàm lượng các tạp chất c, s, Si, Mn,... có trong gang, bằng cách oxi hoá các tạp chất đó thành oxit rồi biến thành xỉ và tách ra khỏi thép. Các phương pháp luyện thép Phương pháp Bet-xơ-me : Phưong pháp Bet-xơ-me luyện thép trong lò thổi có hình quả lê, vỏ ngoài bằng thép, bên trong lát gạch chịu lửa đi-nat (hình 7.3). Luồng không khí mạnh thổi vào gang lỏng, đốt cháy các tạp chất trong gang tạo thành thép trong thời gian ngắn. Nhược điểm của phương pháp Bet-xơ-me là không luyện được thép từ gang chứa nhiều photpho và không luyện được thép có thành phần theo ý muốn. Không khí nén Phương pháp Mac-tanh : Quá trình luyện thép kéo dài 6 - 8 giờ nên người ta có thể phân tích được sản phẩm và cho thêm những chất cần thiết để chế được các loại thép có thành phần mong muốn (hình 7.4). Nhiên liệu kh Cửa nạp nguyên liệu Hình 7.4. Sơ đồ lò 'Mac-tanh xỉ nóng chảy Thép nóng chảy Phương pháp lò điện : Nhiệt lượng sinh ra trong lò hồ quang điện (hình 7.5) giữa các điện cực bằng than chì và của gang lỏng tạo ra nhiệt độ cao hơn và dễ điều chỉnh hơn so với các loại lò trên. Phương pháp lò điện có ưu điểm là luyện được những loại thép đặc biệt mà thành phần có những kim loại khó nóng chảy như vonfam, molipđen, crom,... và không chứa những tạp chất có hại như lưu huỳnh, photpho. Điện cực bằng than chl Cửa nạp nguyên liệu Thép nóng chảy Nhược điểm của lò điện là dung tích nhỏ. BÀI TẬP Nêu những phản ứng chính xảy ra trong lò cao. Nêu các phương pháp luyện thép và cho biết ưu điểm, nhược điểm của mỗi phương pháp. Một loại quặng chứa sắt trong tự nhiên đã được loại bỏ tạp chất. Hoà tan quặng này trong dung dịch HNO3 thấy có khí màu nâu bay ra, dung dịch thu được cho tác dụng với dung dịch BaCI2 thấy có kết tủa trắng (không tan trong axit mạnh). Loại quặng đó là A. xiđerit. B. hematit. c. manhetit. D. pirit sắt. Để khử hoàn toàn 17,6 gam hỗn hợp gồm Fe, FeO, Fe3O4, Fe2O3 đến Fe cần vừa đủ 2,24 lít khí CO (đktc). Khối lượng sắt thu được là A. 15 gam. c. 17 gam. B. 16 gam. D. 18 gam. Nung một mẫu thép thường có khối lượng 10 gam trong 02 dư thu được 0,1568 lít khí co2 (đktc). Thành phần phần trăm theo khối lượng của cacbon trong mẫu thép đó là A. 0,82%. B. 0,84%. c. 0,85%. D. 0,86%. Cần bao nhiêu tấn quặng manhetit chứa 80% Fe3O4 để có thể sản xuất được 800 tấn gang có hàm lượng sắt là 95%. Biết rằng trong quá trình sản xuất, lượng sắt bị hao hụt là 1%.