Giải Hóa 8 - Bài 22: Tính theo phương trình hóa học
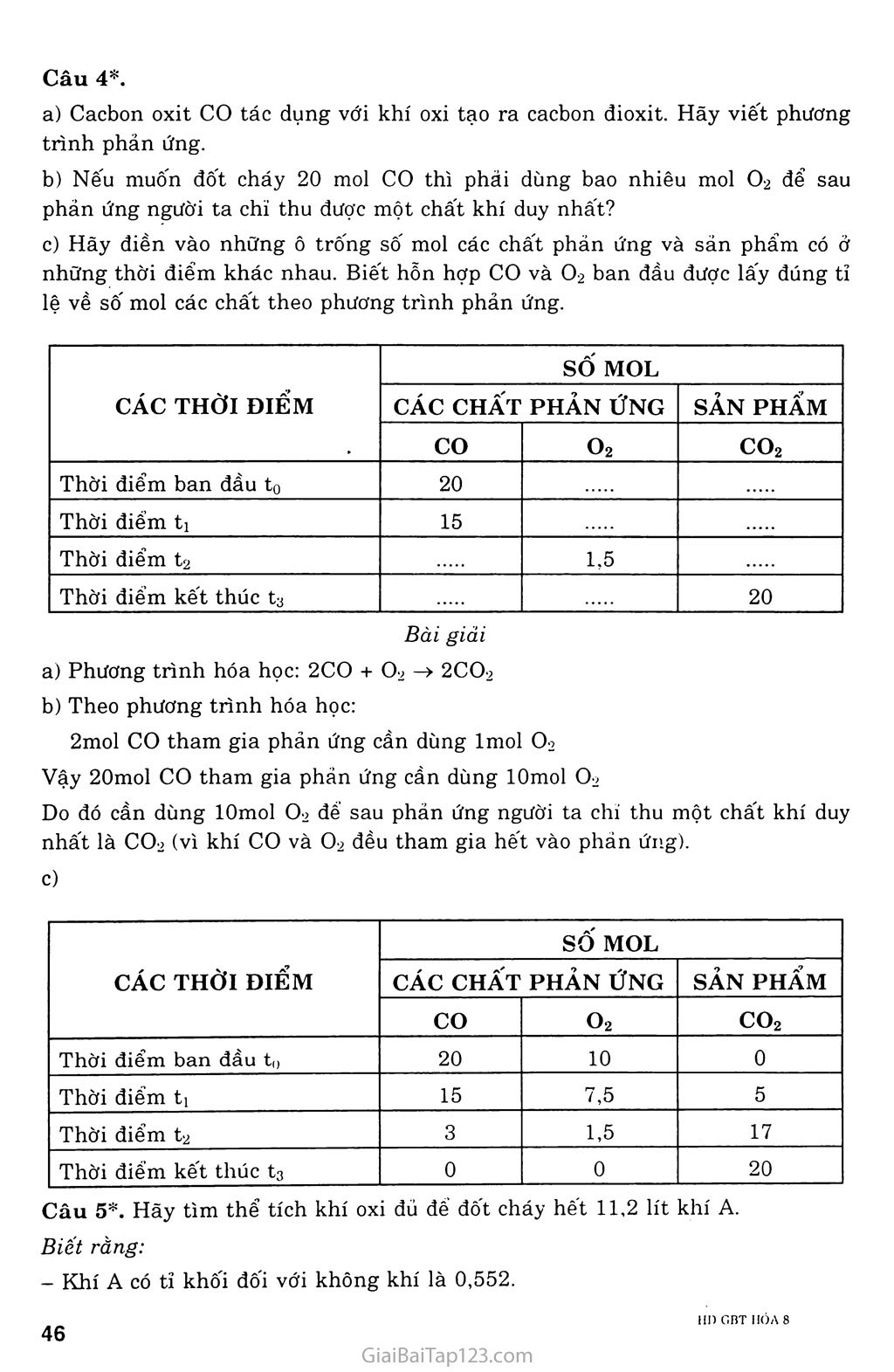
Bài 22. TÍNH THEO PHƯƠNG TRÌNH HÓA HỌC KIẾN THỨC CẦN NAM vững Ý nghĩa của phương trình hóa học: Phương trình hóa học cho biết: Công thức hóa học của chất tham gia và chất tạọ thành. Tỉ lệ sô' phân tử chất tham gia và chất tạo thành. Tính sô' mol hoặc khôi lượng hoặc thể tích các chất tham gia và sản phẩm, gồm 4 bước: Bước 1. Viết phương trình hóa học: Viết đúng cấu tạo hóa học của các chất tham gia và tạo thành. Chọn hệ sô' phân tử sao cho sô' nguyên tử của mỗi nguyên tô' ở hai vê' đều bằng nhau. Bước 2. Chuyển đổi khôi lượng chất hoặc thế tích chất khí thành sô' mol chất. Yêu cầu sử dụng thành thạo các công thức: m _ ™ _ V n = “, m = n.M, n = --- - M 22,4 Bước 3. Dựa vào phương trình hóa học để tìm sô' mol chất tham gia hoặc chất tạo thành. Bước 4. Chuyển đổi sô' mol thành khôi lượng (m = n.M) hoặc thể tích khí ở đktc (V = 22,4 X n). GIẢI BÀI TẬP SÁCH GIÁO KHOA Câu 1. Sắt tác dụng với axit clohiđric: Fe + 2HC1 -> FeCl2 + H2 Nếu có 2,8 gam sắt tham gia phản ứng, em hây tìm: Thể tích khí hiđro thu được ở điều kiện tiêu chuẩn. Khối lượng axit clohiđric cần dùng. Bài giải Phương trình hóa học: Fe + 2HC1 -> FeCl2 + H2T 2 8 Sô' mol của sắt tham gia phản ứng: nFe = = 0,05(mol) 56 Theo phương trình hóa học: Imol Fe tham gia phản ứng thì thu được lmol H2 Vậy 0,05mol Fe tham gia phản ứng thì thu được 0,05mol H2. Thê tích khí H2 thu được ở đktc: Vj,2 = 22,4. nHj = 22,4 X 0,05 = 1,12 (lít). Theo phương trình hóa học: Imol Fe tham gia phản ứng cần dùng 2mol HC1 Vậy 0,05mol Fe tham gia phản ứng cần dùng O,lmol HC1 Khối lượng axit clohiđric cần dùng: niHC! — ưHCi-M-Hci — 0,1.36,5 = 3,65 (gam). Câu 2. Lưu huỳnh s cháy trong không khí sinh ra chất khí mùi hắc, gây ho, đó là khí lưu huỳnh đioxit (khí sunturơ) có công thức hóa học là SƠ9. Viết phương trình hóa học cúa lưu huỳnh cháy trong không khí. Biết khối lượng lưu huỳnh tham gia phản ứng là 1,6 gam. Hãy tìm: Thể tích khí suníùrơ sinh ra ở đktc. Thế tích không khí cần dùng ở đktc. Biết khí oxi chiếm 1/5 thế tích của không khí. Bài giải Phương trình hóa học: s + 02 —> SO2 Số mol của lưu huỳnh tham gia phản ứng: Ils = - 7~’Ệ = 0,05 (mol) Ms 32 Theo phương trình hóa học: Imo] s tham gia phản ứng sinh ra Imol SO9 Vậy 0,05mol tham gia phản ứng sinh ra 0,05mol SO-2 Thế tích khí suníùrơ sinh ra ở đktc: VSO2 = 22,4. nC02 = 22,4 X 0,05 = 1,12 (lít) Theo phương trình hóa học: Imol s tham gia phản ứng cần Imol 02 Vậy 0,05mol s tham gia phản ứng cần 0,05mol O9 Thế’ tích oxi cần dùng ở đktc: VOj = 22,4. nOz = 22,4 X 0,05 = 1,12 (lít). Thể tích không khí cần dùng ở đktc: vkk = 5 Vo = 5 X 1,12 = 5,6 (lít) Câu 3. Có phương trình hóa học sau: CaCO3(r) _c> CaO (r) + co2 (k) Cần dùng bao nhiêu mol CaCO3 đế điều chê được 11,2 gam CaO? Muôn điều chế được 7 gam CaO cần dùng bao nhiêu gain CaCO3? Nêu có 3,5 mol CaCO3 tham gia phản ứng sẽ sinh ra bao nhiêu lít co2 (đktc)? Nếu thu được 13,44 lít khí co2 ở đktc thì có bao nhiêu gam chất rắn tham gia và tạo thành sau phản ứng? Bài giải Phương trình hóa học: CaCO3 CaO + CO2T Sô mol của CaO sinh ra: n(;a() = - 0,2 (mol) . : M,„, 40 + 16 Theo phương trình hóa học: lmol CaCO3 tham gia phản ứng sinh ra Imol CaO Vậy 0,2mol CaCO3 tham gia phản ứng sinh ra 0,2mol CaO. Sô' mol của CaO điều chế được: nCaO = ^°- = . 7 „ = 0,125 (mol) MCa0 40 + 16 Theo phương trình hóa học: lmol CaCO3 tham gia phản ứng, điều chế được Imol CaO Vậy 0,125mol CaCO3 tham gia phản ứng, điều chế được 0,125mol CaO. Khối lượng CaCO3 cần dùng: mcaC0;, = nCaC03. MCaC0;t = 0,125 X 100 - 1,25 (gam) Theo phương trình hóa học: lmol CaCO3 tham gia phản ứng sinh ra 1 mol co2 Vậy 3,5mol CaCO3 tham gia phản ứng sinh ra 3,5mol co2 Thể tích co2 sinh ra ở đktc: VCO2 = 22,4. nc0 = 22,4 X 3,5 = 78,4 (lít) V 13.44 Sô' mol COosinh ra: nco - = J-’ = 0,6 (mol) c°2 • 22,4 22,4 Theo phương trình hóa học: lmol CaCO3 tham gia phản ứng sinh ra Imol co2 Vậy 0,6mol CaCO3 tham gia phản ứng sinh ra 0,6mol co2 Khối lượng CaCO3 tham gia phản ứng là: mCaco3 = nCaC03 • MCaCO3 = °-6 X 100 = 60 (gam)- Theo phương trình hóa học: Imol co2 sinh ra cũng tạo ra Imol CaO Vậy 0,6mol co2 sinh ra cũng tạo ra 0,6mol CaO Khối lượng CaO tạo thành: nicao = ncaO-McaO = 0,6 X 56 = 33,6 (gam). Câu 4*. Cacbon oxit co tác dụng với khí oxi tạo ra cacbon đioxit. Hãy viết phương trình phản ứng. Nếu muốn đốt cháy 20 mol co thì phẳi dùng bao nhiêu mol 02 để sau phản ứng người ta chỉ thu được một chất khí duy nhất? Hãy điền vào những ô trống số mol các chất phản ứng và sản phẩm có ở những thời điểm khác nhau. Biết hỗn hợp co và 02 ban đầu được lấy đúng tỉ lệ về số mol các chất theo phương trình phản ứng. CÁC THỜI ĐIẾM SỐ MOL CÁC CHẤT PHẢN ÚNG SẢN PHẨM CO o2 co2 Thời điểm ban đầu to 20 Thời điểm ti 15 Thời điểm t2 1,5 Thời điểm kết thúc t3 20 Bài giải Phương trình hóa học: 2CO + 02 2CO2 Theo phương trình hóa học: 2mol CO tham gia phản ứng cần dùng Imol 02 Vậy 20mol co tham gia phản ứng cần dùng lOmol o2 Do đó cần dùng lOmol o2 đế sau phản ứng người ta chi thu một chất khí duy nhất là co2 (vì khí co và 02 đều tham gia hết vào phản ứng). c) CÁC THỜI ĐIỂM SỐ MOL CÁC CHẤT PHẢN ỨNG SẢN PHẨM CO o2 co2 Thời điểm ban đầu to 20 10 0 Thời điểm ti 15 7,5 5 Thời điểm t2 3 1,5 17 Thời điểm kết thúc t3 0 0 20 Câu 5*. Hãy tìm thể tích khí oxi đủ đê đốt cháy hết 11,2 lít khí A. Biết rằng: - Khí A có tỉ khối đô'i với không khí là 0,552. - Thành phần theo khối lượng của khí A là: 75%c và 25%H Các thể tích khí đo ở đktc. Bài giải Ta có: ctvkk = 0,552 —> Ma = (ỈA/kk-29 = 0,552 X 29 = 16 Gọi công thức hóa học của khí A là CxHy 75%. 16 _ 12.100% “ %C.Mc H Do đó: X = ' Mc.100% 25%. 16 Â 1.100% %H.MCjHy y = Mh.100% Vậy công thức hóa học của khí A là CH4. Phương trình hóa học: CH4 + 2O2 -> co2 + 2H2O ch4 V 119 Sô' moi của khí CH4 là: nCH = = __ - 0,5(mol) CHí 22,4 22,4 Theo phương trình hóa học: lmol CH4 tham gia phản ứng cần dùng 2mol 02 Vậy 0,5mol CH4 tham gia phản ứng cần dùng lmol O2 Thể tích khí O2 cần dùng: V0’2 = n02.22,4 = 1 X 22,4 = 22,4 (Z).