SGK Hóa Học 11 - Bài 25: Ankan
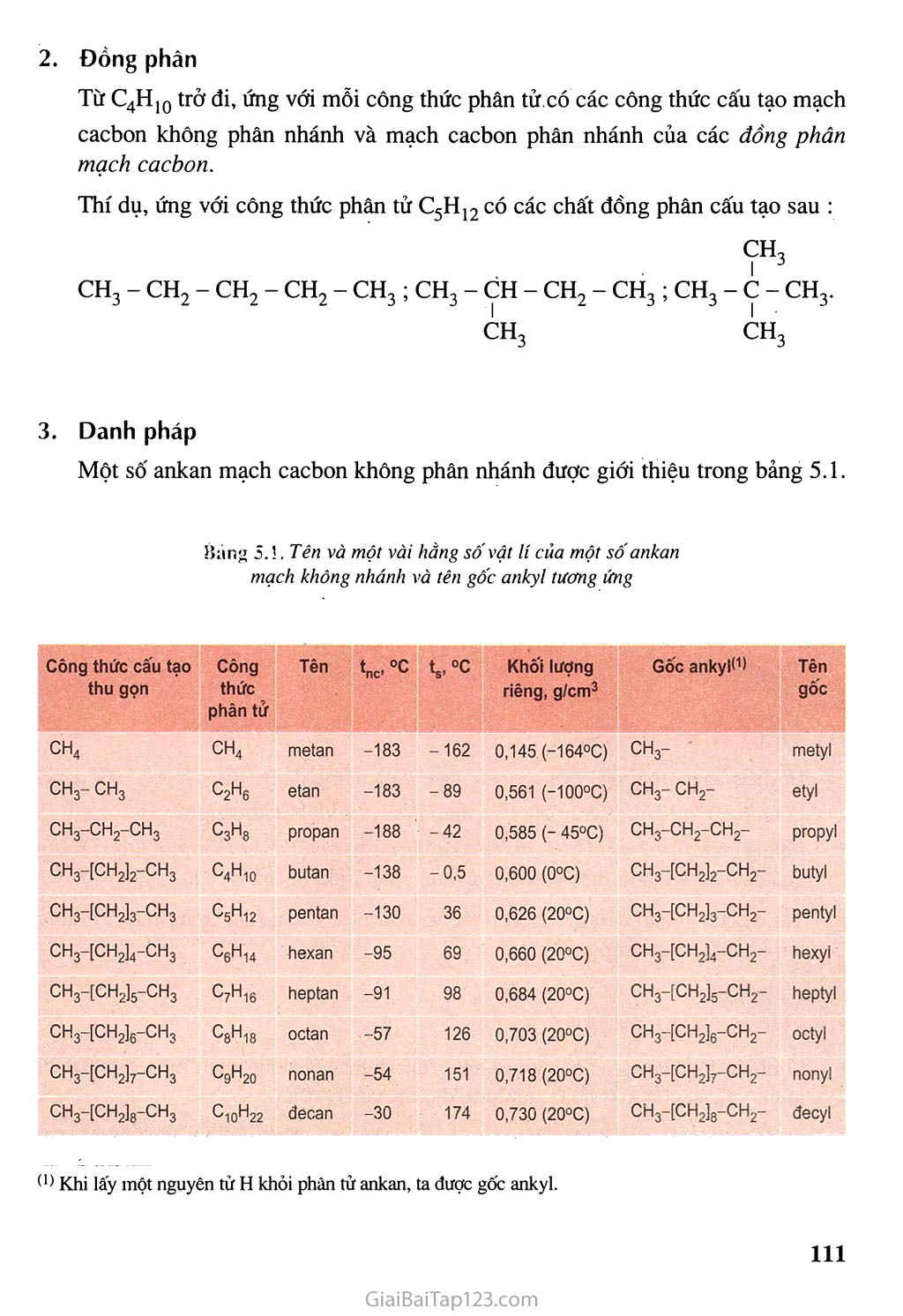
Chương MPRQCACBoaf NO Thế nào là ankan, xicỉoankan ? Chúng có điểm gì giống nhau và khác nhau về cấu tạo và tính chất ? Các ankan được ứng dụng trong những lĩnh vực nào ? Các nguồn hiãrocacbon no trong tự nhiên. Nhè máy lọc hoá dầu Hiđrocacbon no là hiđrocacbon mà trong phân tử chỉ có liên kết đơn. Hiđrocacbon no được chia thành hai loại: Ankan (hay parafin) là những hiđrocacbon no không có mạch vòng. Xicloankan là những hiđrocacbon no có mạch vòng. Hiđrocacbon no là nguồn nhiên liệu chính và là nguồn nguyên liệu quan trọng trong ngành công nghiệp hoá học. ANKAN & Biết viết công thức cấu tạo và gọi tên một số ankan đon giản. & Biết tính chất hoá học đặc trưng cúa ankan là phản ứng thế. & Biết được tầm quan trọng cúa hiđrocacbon no trong công nghiệp và trong đời sống. I - ĐỒNG ĐẲNG, ĐỒNG PHÂN, DANH PHÁP Dãy đồng đẳng ankan Metan (CH4) và các chất tiếp theo có công thức phân tử CọH6, CjHg, C4H10, C5H12,.. lập thành dãy đồng đẳng ankan (hay parafin) có công thức chung CnH2n+2 (n - 1 )• Trong phân tử ankan chỉ có các liên kết đơn c - c, c - H. Mỗi nguyên tử cacbon tạo được 4 liên kết đơn hướng từ nguyên tử c (nằm ở tâm của hình tứ diện) về 4 đỉnh của một tứ diện với góc liên kết ccc 5 HCH 5 CCH khoảng 109,5°. Do đó, các nguyên tử cacbon trong phân tử ankan (trừ C2H6) không cùng nằm trên một đường thẳng. Hình 5.1. Mô hình phân tử butan (a) và isobutan (b) Đồng phân Từ C4H10 trở đi, ứng với mỗi công thức phân tử có các công thức cấu tạo mạch cacbon không phân nhánh và mạch cacbon phân nhánh của các đồng phân mạch cacbon. Thí dụ, ứng với công thức phân tử C5Hj, có các chất đồng phân cấu tạo sau : CH, • I __ CH3 - CH, - CH, - CH2 - CH3; CH3 - CH - CH2 - CH3 ; CH3 - C - CH3. CH3 ch3 Danh pháp Một số ankan mạch cacbon không phân nhánh được giới thiệu trong bảng 5.1. Bàng 5. Ị. Tên và một vài hắng số vật lí của một số ankan mạch không nhánh và tên gốc ankyl tương ứng Công thức cấu tạo thu gọn Công thức phân tử Tên °C ts, °C Khối lượng riêng, g/cm3 Gốc ankylhl Tên gốc ch4 ch4 metan -183 -162 0,145 (-164°C) CH3- metyl ch3- ch3 c2h6 etan -183 -89 0,561 (-100°C) ch3- ch2- etyl ch3-ch2-ch3 C3H8 propan -188 -42 0,585 (- 45°C) ch3-ch2-ch2- propyl CH3-[CH2]2-CH3 C4H10 butan -138 -0,5 0,600 (0°C) CH3-[CH2]2-CH2- butyl CH3-[CH2]3-CH3 C5H12 pentan -130 36 0,626 (20°C) CH3-[CH2]3-CH2- pentyl CH3-[CH2]4-CH3 CbHi4 hexan -95 69 0,660 (20°C) CH3-[CH2]4-CH2- hexyi CH3-[CH2]5-CH3 ^7H16 heptan -91 98 0,684 (20°C) CH3-[CH2]5-CH2- heptyl CH3-[CH2]6-CH3 ^8^18 octan -57 126 0,703 (20°C) CH3-[CH2]6-CH2- octyl CH3-[CH2]7-CH3 CgH20 nonan -54 151 0,718 (20°C) CH3-[CH2]7-CH2- nonyl CH3-[CH2]8-CH3 c10h22 đecan -30 174 0,730 (20°C) CH3-[CH2]8-CH2- đecyl (!) Khi lấy một nguyên tử H khỏi phân tử ankan, ta được gốc ankyl. Các ankan có mạch nhánh được gọi tên theo danh pháp thay thế như sau : Chọn mạch cacbon dài nhất và có nhiều nhánh nhất làm mạch chính. Đánh số thứ tự các nguyên tử cacbon mạch chính từ phía gần nhánh hơn. Gọi tên mạch nhánh (nhóm ankyl) theo thứ tự vần chữ cái cùng với số chỉ vị trí của nó, tiếp theo là tên ankan tương ứng với mạch chính (xem bảng 5.1). Thí dụ : CH3 - CH - CH2 - CH3 CH, 2-metylbutan (isopentan) CH3 1 21 CH, - c - CH, 5 I j ch3 2,2-đimetylpropan (neopentan) Một số chất CÓ tên thông thường, thí dụ : isopentan, neopentan,... Bậc của nguyên tử c trong phân tử hiđrocacbon no được tính bằng số liên kết của nó với các nguyên tử cacbon khác. Till dụ : Trong phân tử 2-metylbutan, bậc của các nguyên tử c số 1 và số 4 là I; bậc của nguyên tử c số 3 là II; bậc của nguyên tử c số 2 là III. Trong phân tử 2,2-đimetylpropan, bậc của nguyên tử c số 2 là IV. - TÍNH CHẤT VẬT LÍ 0 điều kiện thường, bốn ankan đầu dãy đồng đẳng (từ CH4 đến C4H10) là những chất khí, các ankan tiếp theo là chất lỏng, từ khoảng CjgH38 trở đi là những chất rắn. Nói chung, nhiệt độ nóng chảy, nhiệt độ sôi và khối lượng riêng của các ankan tăng theo chiều tăng của phân tử khối (bảng 5.1). Tất cả các ankan đều nhẹ hơn nước và hầu như không tan trong nước, nhưng tan nhiều trong dung mói hữu cơ. - TÍNH CHẤT HOÁ HỌC Ở nhiệt độ thường, các ankan không tác dụng với dung dịch axit, dung dịch kiềm và các chất oxi hoá như dung dịch KMnO4 (thuốc tím)... Khi chiếu sáng hoặc đun nóng, các ankan dễ dàng tham gia các phản ứng thế, phản ứng tách hiđro và phản ứng cháy. 1. Phản ứng thê bởi halogen Clo có thể thay thế lần lượt từng nguyên tử H trong phân tử metan : ch4 + Cl2 1 r'i as -> CH3C1 clometan (metyl clorua) V r^T T /"■■’I + HC1 as dl^Cl 1 CỈ2 4- MCI điclometan (metylen clorua) CH2C12+ Cl2 as -> CHC13 + HCl triclometan (clorofom) chci3 + Cl2 as -> CC14 + HC1 tetraclometan (cacbon tetraclorua) Các đồng đẳng của metan cũng tham gia phản ứng thế tương tự metan. Thí dụ : CH3CH2CH2C1 + HC1 CH3CH2CH3 + Cl2^<^ 1-clopropan (43%) CH.-CH-CH. + HC1 L C1 2-clopropan (57%) Nhận xét: Nguyên tử hiđro liên kết với nguyên tử cacbon bậc cao hơn dễ bị thè'hơn nguyên lử hiđro liên kết với nguyên tử cacbon bậc thấp hơn. Các phản ứng trên được gọi là phản ứng halogen hoá. Các sản phẩm thế được gọi là dẫn xuất halogen của hiđrocacbon. 2. Phán ứng tách Dưới tác dụng của nhiệt và chất xúc tác thích hợp, các ankan có phân tử khối nhỏ bị tách hiđro thành hiđrocacbon không no tương ứng : Thí dụ-. CH3-CH3 500°C’xt > CH2 = CH2 + H2 Ở nhiệt độ cao và có mặt chất xúc tác thích hợp, ngoài việc bị tách hiđro, các ankan còn có thể bị phân cắt mạch cacbon tạo thành các phân tử nhỏ hơn. Thí dụ : ch4 + c3h6 ch3 - ch2 - ch2 - ch3 t°, xt C-,H4 + CọHg c4h8 + h2 Phản úng oxi hoá Khi bị đốt, các ankan đều cháy, toả nhiều nhiệt : C„H2nt2 + 02 nco2 + (n+1)H2O Nếu thiếu oxi, phản ứng cháy của ankan xảy ra không hoàn toàn : sản phẩm cháy ngoài COọ, H2O còn có c, co,... - ĐIỀU CHÊ Trong phòng thí nghiệm Metan được điều chế bằng cách đun nóng natri axetat khan với hỗn hợp vôi tôi xút (hình 5.2) : CH3COONa + NaOH - Ca0---0--> CH4t + Na2CO3 Trong công nghiệp Các ankan là thành phần chính của dầu mỏ, khí thiên nhiên và khí mỏ dầu. Từ dầu mỏ, bằng phương pháp chưng cất phân đoạn, ta thu được các ankan ở các phân đoạn khác nhau. Từ khí thiên nhiên và khí mỏ dầu cũng thu được các ankan CH4, Ọ,H6, CjHg, C4H, Q,... ỨNG DỤNG CỦA ANKAN Các ankan có ứng dụng trong nhiều lĩnh vực khác nhau : lằm nhiên liệu, nguyên liệu cho công nghiệp. BÀI TẬP 1. 2. Thế nào là hiđrocacbon no, ankan, xicloankan ? Viết công thức phân tử của các hiđrocacbon tương ứng với các gốc ankyl sau : _CH3, -C3H7 , -C6H13. Viết phương trình hoá học của qác phản ứng sau : Propan tác dụng với clo (theo tỉ lệ mol 1:1) khi chiếu sáng. Tách một phân tử hiđro từ phân tử propan. Đốt cháy hexan. Các hiđrocacbon no được dùng làm nhiên liệu là do nguyên nhân nào sau đây ? Hiđrocacbon no có phản ứng thế. Hiđrocacbon no có nhiều trong tự nhiên, c. Hiđrocacbon no là chất nhẹ hơn nước. D. Hiđrocacbon no cháy toả nhiều nhiệt và có nhiều trong tự nhiên. Hãy giải thích : Tại sao không được để các bình chứa xăng, dầu (gồm các ankan) gần lửa, trong khi'đó người ta có thể nấu chảy nhựa đường (trong thành phần cũng có các ankan) để làm đường giao thông. Không dùng nước để dập các đám cháy xăng, dầu mà phải dùng cát hoặc bình chứa khí cacbonic. Công thức cấu tạo CH3-CH -CH2 -CH2 -CH3 ứng với tên gọi nào sau đây ? CHg neopentan 2-metylpentan c. isobutan D. 1,1-đimetylbutan Khi đốt cháy hoàn toàn 3,60g ankan X thu được 5,60 lít khí co2 (đktc). Công thức phân tử của X là C3H8 C5H10 c. C5H12 D. C4H10