SGK Hóa Học 11 - Bài 41: Phenol
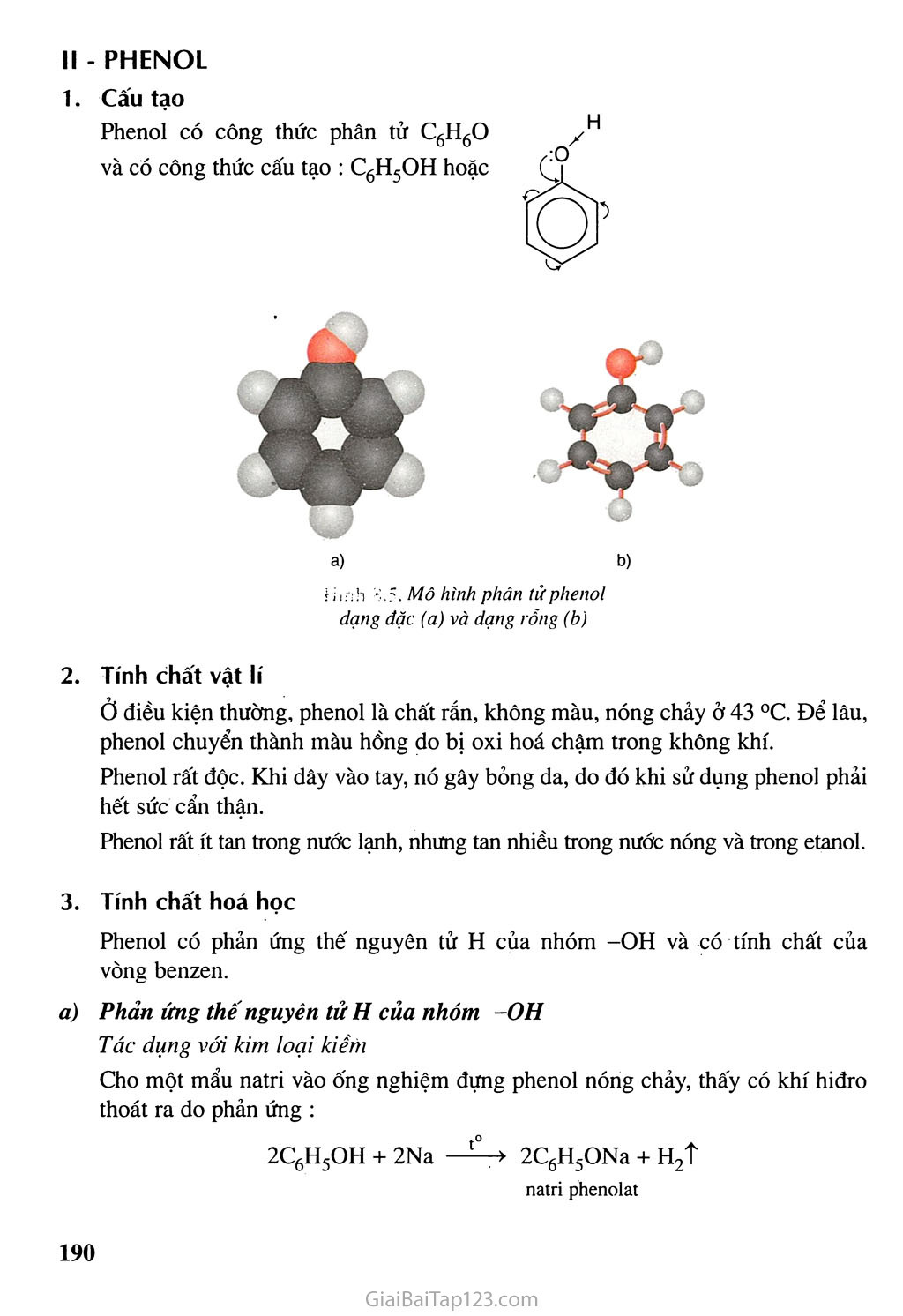
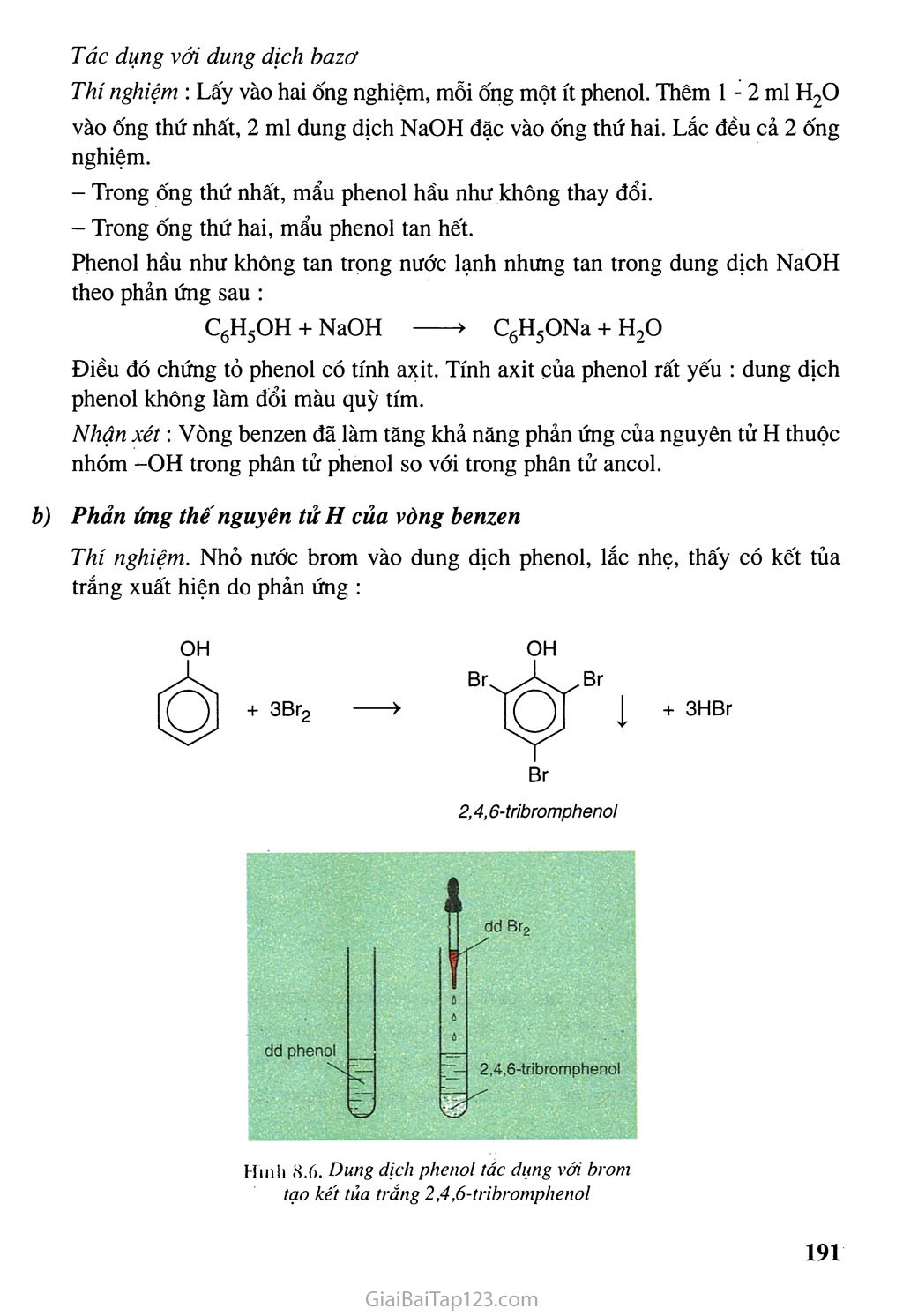
Bài PHENOL £7 Biết khái niệm về loại họp chất phenol. £7 Biết cấu tạo, tính chất của phenol đơn gián nhất. I - ĐỊNH NGHĨA, PHẢN LOẠI Định nghĩa Phenol là những hợp chất hữu cơ trong phân tử có nhóm -OH liên kết trực tiếp với nguyên tử cacbon của- vòng benzen. Nhóm -OH liên kết trực tiếp với nguyên tử cacbon của vòng benzen được gọi là -OH phenol. 2. Phenol đơn giản nhất là C6H5-OH, phân tử gồm một nhóm -OH liên kết với gốc phenyl. Phân loại Dựa theo số nhóm -OH trong phân tử, các phenol được phân loại thành : Phenol đơn chức : Phân tử có mệt nhóm -OH phenol. Thí dụ : Phenol đa chức : Phân tử có hai hay nhiều nhóm -OH phenol. Thí dụ : OH Ố OH OH ộ: ©ở phenol |4 ch3 4-metylphenol a-naphtol II - PHENOL Câu tạo Phenol có công thức phân tử C6H6O và cố công thức cấu tạo : C6H5OH hoặc o a) b) Mô hình phán tử phenol dạng đặc (a) và dạng rỗng (b) Tính chất vật lí O điều kiện thường, phenol là chất rắn, không màu, nóng chảy ở 43 °C. Để lâu, phenol chuyển thành màu hồng do bị oxi hoá chậm trong không khí. Phenol rất độc. Khi dây vào tay, nó gây bỏng da, do đó khi sử dụng phenol phải hết sức cẩn thận. Phenol rất ít tan trong nước lạnh, nhưng tan nhiều trong nước nóng và trong etanol. Tính chất hoá học Phenol có phản ứng thế nguyên tử H của nhóm -OH và có tính chất của vòng benzen. Phản ứng thê' nguyên tử H của nhóm -OH Tác dụng với kim ỉoại kiềm Cho một mẩu natri vào ống nghiệm đựng phenol nóng chảy, thấy có khí hiđro thoát ra do phản ứng : 2C6H5OH + 2Na ——> 2C6H5ONa + H2t natri phenolat Tác dụng với dung dịch bazơ Thí nghiệm : Lấy vào hai ống nghiệm, mỗi ống một ít phenol. Thêm 1 - 2 ml H2O vào ống thứ nhất, 2 ml dung dịch NaOH đặc vào ống thứ hai. Lắc đều cả 2 ống nghiệm. Trong ống thứ nhất, mẩu phenol hầu như không thay đổi. Trong ống thứ hai, mẩu phenol tan hết. Phenol hầu như không tan trong nước lạnh nhưng tan trong dung dịch NaOH theo phản ứng sau : C6H5OH + NaOH > C6H5ONa + H2O Điều đó chứng tỏ phenol có tính axit. Tính axit của phenol rất yếu : dung dịch phenol không làm đổi màu quỳ tím. Nhận xét: Vòng benzen đã làm tăng khả năng phản ứng của nguyên tử H thuộc nhóm -OH trong phân tử phenol so với trong phân tử ancol. b) Phản ứng thế nguyên tử H của vòng benzen Thí nghiệm. Nhỏ nước brom vào dung dịch phenol, lắc nhẹ, thấy có kết tủa trắng xuất hiện do phản ứng : OH OH Br 2,4,6-tribromphenol . Dưng dịch phenol tác dụng với brom tạo kết tủa trắng 2,4,6-tribromphenol Nếu cho dung dịch HNO3 vào dung dịch phenol, thấy có kết tủa vàng của 2,4,6-trinitrophenol (axit picric). Nhận xét: Nguyên tử H của vòng benzen trong phân tử phenol dễ bị thay thế hơn nguyên tử H của vòng benzen trong phân tử các hiđrocacbon thơm. Đó là do ảnh hưởng của nhóm -OH tới vòng benzen. Ảnh hưởng của vòng benzen đến nhóm -OH và ảnh hưởng của nhóm -OH đến vòng benzen được gọi là ảnh hưởng qua lại giữa các nguyên tử trong phân tử. Điều chế Trong công nghiệp, hiện nay phenol được điều chế bằng cách oxi hoá cumen (isopropylbenzen) nhờ oxi không khí, sau đó thuỷ phân trong dung dịch IÍ2SO4 loãng. Sản phẩm thu được gồm phenol và axeton. Đun nóng cho axeton bay hơi rồi ngưng tụ hơi thu lấy axeton, còn lại là phenol. Phenol cũng có thể được điều chế từ benzen theo sơ đồ : C6H6 > C6H5Br —> C6H5ONa > C6H5OH Ngoài ra, một lượng đáng kể phenol được tách ra từ nhựa than đá trong quá trình luyện cốc. Úng dụng Phenol là nguyên liệu sản xuất nhựa phenol-fomandehit hay poli(phenol- fomandehit) dùng chế tạo các đồ dân dụng ; nhựa ure-fomanđehit dùng làm chất kết dính (như keo dán gỗ, dán kim loại, sành, sứ...). chất diệt cỏ 2,4-D (ci Phenol còn được dùng để sản xuất phẩm nhuộm, thuốc nổ (2,4,6-trinứrophenol), CI o - CHgCOOH ì chất diệt nấm mốc (niưophenol),... BÀI TẬP 1. □ □ □ □ Ghi Đ (đúng) hoặc s (sai) vào ô trống bên cạnh các câu sau : a) Phenol C6H5-OH là một rượu thơm. Phenol tác dụng được với natri hiđroxit tạo thành muối và nước. Phenol tham gia phản ứng thế brom và thế nítro dễ hơn benzen. Dung dịch phenol làm quỳ tím hoá đỏ do nó là axit. Giữa nhóm -OH và vòng benzen trong phân tử phenol có ảnh hưởng qua lại lẫn nhau. Từ benzen và các chất vô cơ cần thiết có thể điểu chế được các chất sau : 2,4,6-tribromphenol (1); 2,4,6-trinitrophenol (2). Viết phương trình hoá học của các phản ứng xảy ra. Cho 14,0 gam hỗn hợp A gồm phenol và etanol tác dụng với natrí dư thu được 2,24 lít khí hiđro (đktc). Viết các phương trình hoá học của các phản ứng xảy ra. Tính thành phần phần trăm khối lượng của mỗi chất trong A. Cho 14,0 gam hỗn hợp A tác dụng với dung dịch HNO3 (đủ) thì thu được bao nhiêu gam axit picric (2,4,6-trinitrophenol) ? Cho từ từ phenol vào nước brom (1) ; stiren vào dung dịch brom trong CCI4 (2). Nêu hiện tượng và viết các phương trình hoá học. Sục khí co2 vào dung dịch natrí phenolat thấy dung dịch bị vẩn đục, trong dung dịch có NaHCO3 được tạo thành. Viết phương trình hoá học của phản ứng xảy ra và giải thích. Nhận xét về tính axít của phenol. Viết các phương trình hoá học điểu chế: phenol từ benzen (1), stiren từ etylbenzen (2). Các chất vô cơ cần thiết coi như có đủ. / •