SGK Hóa Học 9 - Bài 32: Luyện tập chương 3: Phi kim - Sơ lược về bảng tuần hoàn các nguyên tố hóa học
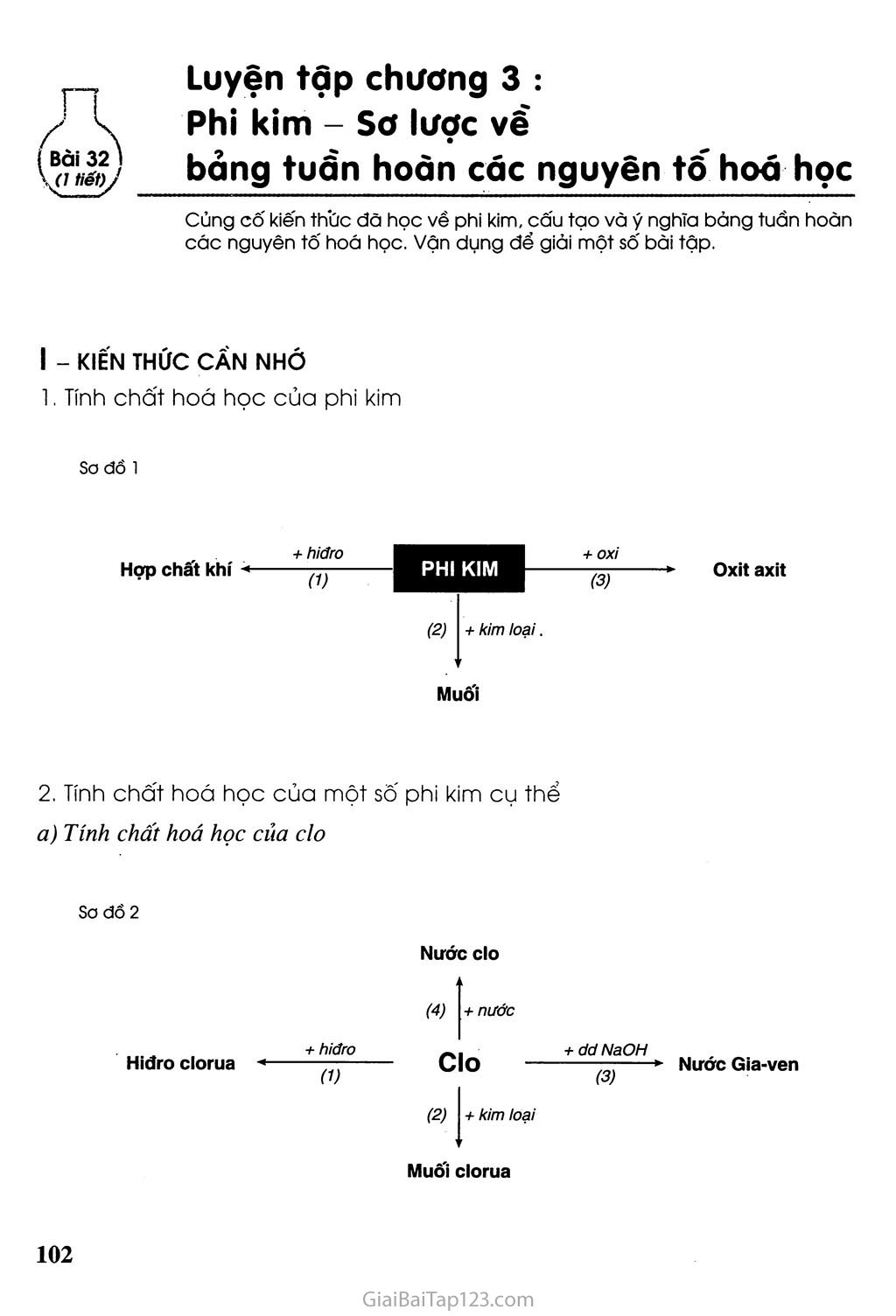
ẽ Luyện tập chương 3 : Phi kim - Sơ lược về bảng tuần hoàn các nguyên tố hoáhọc Củng cố kiến th'ũc đã học về phi kim, cấu tạo và ý nghĩa bâng tuần hoàn các nguyên tố hoá học. Vận dụng để giãi một số bài tập. I - KIẾN THỨC CẦN NHÓ 1. Tính chất hoá học của phi kim Sơ dồ 1 Hợp chất khí + hiđro (1) PHI KIM (3) Oxit axit (2) + kim loại. Muối 2. Tính chốt hoá học của một số phi kim cụ thể Tính chất hoá học của clo Sơ đổ 2 Nước clo (4) + nước Hiđro clorua + hiđro Clo + dd NaOH (3) ' Nước Gia-ven (2) + kim loại Muối clorua Tính chất hoá học của cacbon và hợp chất của cacbon Sơ đổ 3 Bảng tuần hoàn các nguyên tố hoá học Cấu tạo bảng tuần hoàn Ô nguyên tố. Chu kì. Nhóm. Sự biến đổi tính chất của các nguyên tố trong bảng tuần hoàn. Ý nghĩa của bảng tuần hoàn. II - BÀI TẬP Căn cứ vào sơ đồ 1, hãy viết các phương trình hoá học với phi kim cụ thể là lưu huỳnh. Hãy viết các phương trình hoá học biểu diễn tính chất hoá học của clo theo sơ đồ 2. Hãy viết các phương trình hoá học biểu diễn tính chất hoá học của cacbon và một số hợp chất của nó theo sơ đổ 3. Cho biết vai trò của cacbon trong các phản ứng đó. Nguyên tố A có sô' hiệu nguyên tử là 11, chu kì 3, nhóm I trong bảng tuần hoàn các nguyên tố hoá học. Hãy cho biết: Cấu tạo nguyên tử của A. Tính chất hoá học đặc trưng của A. So sánh tính chất hoá học của A với các nguyên tố lân cận. a) Hãy xác định công thức của một loại oxit sắt, biết rằng khi cho 32 gam oxit sắt này tác dụng hoàn toàn với khí cacbon oxit thì thu được 22,4 gam chất rắn. Biết khối lượng mol phân tử của oxit sắt là 160 gam/mol. b) Chất khí sinh ra được hấp thụ hoàn toàn bằng nước vôi trong dư. Tính khối lượng kết tủa thu được. Cho 69,6 gam MnO2 tác dụng với dung dịch HCi đặc dư thu được một lượng khí X. Dần khí X vào 500 ml dung dịch NaOH 4M thu được dung dịch A. Tính nồng độ mol của các chất trong dung dịch A. Giả thiết rằng thể tích dung dịch sau phản ứng thay đổi không đáng kể.