Giải Hóa 11 - Bài 29: Ankin
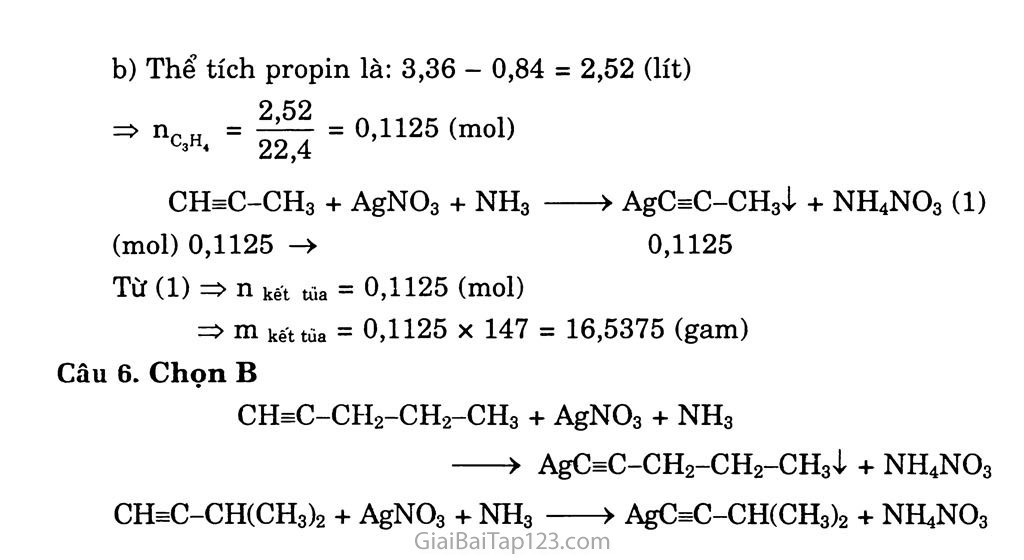
BÀI 29. ANKIN A. KIẾN THỨC CẦN NHỚ I. Đồng đẳng, đồng phân, danh pháp Dãy đồng đẳng ankin Axetilen (CH=CH) và các chất tiếp theo có công thức phân tử C3H4, C4H6)... có tính chất tương tự như axetilen lập thành dãy đồng đẳng của axetilen được gọi là ankin. Công thức phân tử chung của ankin là CnH2n _ 2 (n > 2). Đồng phân Hai chất đầu dãy (C2H2, C3H4) không có đồng phân ankin. Các ankin từ C4H6 trở lên có đồng phân vị trí của liên kết ba, từ C5H8 còn có đồng phân mạch cacbon (tương tự anken). Danh pháp Tên thông thường: Tên gốc ankyl liên kết với nguyên tử c của liên kết ba + axetilen CH=CH CH=C-CH2-CH3 ch3-c=c-ch3 ch3-ch2-ch2-c^ch : axetilen : etylaxetilen : đỉmetylaxetỉlen : propylaxetilen b) Tên hệ thống: Tên thay thế và một vài hằng số vật lí của một số ankin Công thức cấu tạo Tên thay thế tnc,°C ts,°c D g/cm3 (20°C) CH=CH etin - 82 - 75 CHsC- CH3 propin - 101,5 - 23 ch=c-ch2-ch3 but-l-in - 122 8 CH=C-[CH2]2-CH3 pent-l-in - 98 40 0,695 CH=C-[CH2]3-CH3 hex-1-in - 124 72 0,716 CH=C-[CH2]4-CH3 hept-l-in - 80 100 0,733 CHeeC-[CH2]5-CH3 oct-1-in - 70 126 0,746 CH=C-[CH2]6-CH3 non-l-in 151 0,757 CH=C-[CH2]7-CH3 đec-1-in 174 0,766 Tên thay thế của ankin được xuất phát từ tên của ankan có cùng mạch cacbon bằng cách đổi đuôi -an thành -in. Các ankin có liên kết ba ở đầu mạch (dạng R-C=CH) được gọi là các ank-l-in. Etin còn có tên thông thường là axetilen. II. Tính chất hóa học Phản ứng cộng Cộng hiđro Khi hiđro hóa ankin có xúc tác niken, thu được ankan. CnH2n_2+2H2 --^-t0 -> CnH2n + 2 Khi xúc tác là hỗn hợp Pd/PbCO3 hoặc Pd/BaSO4, ankin chỉ cộng một phân tử hiđro tạo thành anken. CHsCH + H2 Pb/Pb9°?.-..t0...> CH2=CH2 Đặc tính này được dùng để điều chế anken từ ankin. Cộng brom, clo Brom và clo cũng tác dụng với ankin theo hai giai đoạn liên tiếp. CH=CH + Br2 dung dịch ► CHBr=CHBr : 1,2-đibronietan CHBr=CHBr + Br2 dung dịch > CHBr2-CHBr2 1,1,2,2-tetrabrometan Cộng HX (X là OH, Cl, Br, CH3COO...) Ankin tác dụng với HX theo hai giai đoạn liên tiếp. CH=CH + HC1 Xt-t0 > CH2=CHC1 (vinyl cìorua) CH2=CHC1 + HC1 —xt,t° > CH3-CHC12 (1,1-dicloetan) GIẢI BÀI TẬP HÓA HỌC 11 - cơ BẲN Khi xúc tác thích hợp, ankin tác dụng với HC1 sinh ra dẫn xuất monoclo anken. CH^CH + HC1 > CH2=CHC1 (vinyl clorua) Phản ứng cộng HX của các ankin cũng tuân theo qựy tắc Mac-côp-nhi-côp. CI CH3-C=CH +hc1 > h3c—c=ch2 ■■ +HC1- > H3C—C—ch3 Cl CI 2,2-điclopropan Phản ứng cộng H2O của các ankin chỉ diễn ra theo tỉ lệ số mol 1 : 1 CH=CH + H2O-T4 > [CH2=CH-OH] tf>hign > CH3-CH=O 80 c anđehit axetic Phản ứng dime và trims hóa Hai phân tử axetilen -> vinylaxetilen: 2CH=CH CuC1't^C1 > CHsC-CH=CH2 Ba phân tử axetilen cộng hợp với nhau tạo thành benzen: qpTJ=pTT 600°C Í^Ỳl bột than hoạt tính Phản ứng thế bằng ion kim loại CH^CH + 2AgNO3 + 2NH3 > AgC^CAgị + 2NH4NO3 Rạc axetilua Chú ý: Các ank-l-in khác như propin, but-l-in, ... cũng có phản ứng tương tự như axetilen. Do đó, tính chất này được dùng để phân biệt ank-l-in với anken và các ankỉn khác. Phản ứng oxi hóa Phản ứng oxi hóa hoàn toàn (cháy) 2CnH2n_2 + (3n - l)02 —2nCO2 + 2(n - 1)H2O Phản ứng oxi hóa không hoàn toàn Tương tự như anken và ankađien thì ankin cũng có khả năng làm mất màu dung dịch KMnO4, do phản ứng oxi hóa không hoàn toàn. 3C2H2 + 8KMnO4 + 4H2O —> -—> 3HOOC-COOH + 8MnO2ị + 8KOH Axií oxalic 3CH3-C=CH + 8KMnO4 + KOH-> > 3CH3-COOK + 3K2CO3 + 8MnO2ị + 2H2O Điều chế Điểu chế đồng đẳng axetilen Từ axetilen CH=CH + Na 150°c > CH^CNa + |h2T 2 CHsCNa + R-X > CH=C-R + NaX Từ. dẫn xuất đihalogen CnH2nBr2 + 2K0H > CnH2n_2 + 2KBr + 2H2O hoặc R-CHX-CHX-R’ - KOht'nrA1 > R-CebC-R’ + 2HX R-CH2-CHX2 K0H/n^ > R-C=CH + 2HX Từ dẫn xuất tetrahalogen R-CX2-CX2-R’ + 2Zn > R-C=C-R’ Điều chế axetilen Từ CH4: 2CH4 làm;"*o?aĩù> > C2H2 + 3H2 1500 c Từ CaC2: CaC2 + 2H2O > Ca(OH)2 + C2H2T CaC2 + 2HC1 > CaCl2 + C2H2T Từ dẫn xuất halogen: C2H2Br4 + 2Zn > C2H2f + 2ZnBr2 C2H4Br2+ 2KOH C2H2T + 2KBr + 2H2O Từ C2Ag2: C2Ag2 + 2HC1 > C2H2T + 2AgClị Tổng hợp trực tiếp: 2C + H2 ——> C2H2. Chú ý: Phản ứng này không áp dụng trong thực tế, chỉ có ý nghĩa về mặt lí thuyết. B. HƯỚNG DẪN GIẢI BÀI TẬP SÁCH GIÁO KHOA TRANG 145 Câu 1. a) CTPT Công thức cấu tạo C4H6 CH^C-CH2-CH3 : but-l-in CH3-CC-CH3 : but-2-in. c5h8 CH=C-CH2-CH2-CH3 : pent-l-in CH3-C=C-CH2-CH3 : pent-2-in CH=C-CH(CH3)2: 3-metyl-but-l-in. b) Tên Công thức cấu tạo Pent-2-in CH3-C = C-CH2-CH3 3-metylpent-l-in HC = C-CH(CH3)-CH2-CH3 2,5-đimetylhex-3-in H3C-CH(CH3)-C = C-CH(CH3)-CH3 Câu 2. CHeeC-CH3 + H2 Pb/pbCCM°-.-> CH2=CH-CH3 CH=C-CH3 + Br2 dư > CHBr2-CBr2-CH3 CH=C-CH3 + AgNO3 + NH3 > CAg=C-CH;4 + NH4NO3 CH=C-CH3 + 2HC1 15»^C ■ > CH3-CCÌ2 CH3 Câu 3. Cho tác dụng với dung dịch AgNO3 trong NH3 dư, chất nào tạo kết tủa thì đó là axetilen, chất nào không tạo kết tủa thì là etilen. Bảng nhận biết: Thuốc thử ch4 CH2=CH2 CHsCH AgNO3/NH3 Không hiện tượng Không hiện tượng Kết tủa vàng nhạt Nước brom Không hiện tượng Nhạt màu Phản ứng: CHsCH + 2AgNO3 + 2NH3 > AgC^CAgị + 2NH4NO3 CH2=CH2 + Br2 ——> CH2Br-CH2Br Câu 4. Chọn c CH2=CH2 + Br2 > CH2Br-CH2Br CH3-C = C-CH3 + 2Br2 > CH3-CBr2 -CBr2-CH3 CH=CH + 2Br2 > CHBr2-CHBr2 Câu 5. a) Khi dẫn hỗn hợp A đi qua dung dịch AgNO3/NH3 (dư) thì propin sẽ tác dụng hết với AgNCVNHs, etilen không tác dụng. Vậy 0,84 lít khí thoát ra là etilen. Vậy: %vr „ = X 100% = 25% C2"4 3,36 b) Thể tích propin là: 3,36 - 0,84 = 2,52 (lít) 9 52 => nr „ = = 0,1125 (mol) c3h4 22,4 CH=C-CH3 + AgNO3 + NH3 > AgC=C-CH3ị + NH4NO3 (1) (mol) 0,1125 -> 0,1125 Từ (1) => n kết tùa = 0,1125 (mol) => m kết tủa = 0,1125 X 147 = 16,5375 (gam) Câu 6. Chọn B CH=C-CH2-CH2-CH3 + AgNO3 + NH3 > AgC=C-CH2-CH2-CH3ị + NH4NO3 CH AgC=C-CH(CH3)2 + NH4NO3