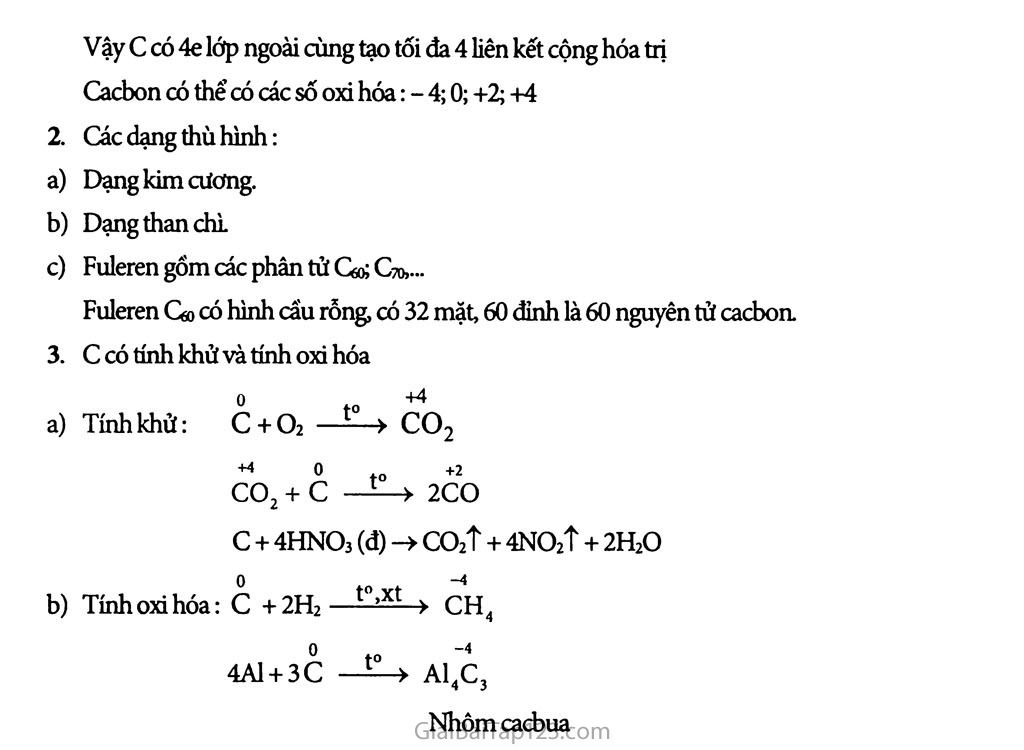Giải bài tập Hóa 11 Bài 15: Cacbon
Chương 3. CACBON - SILIC Bài 15 : Cacbon Cacbon (C) là nguyên tố ở phân nhóm chính nhóm IV (rvA). Cacbon có 6 electron; Cấu hình electron: c: Is2 2s2 2p2 Vậy c có 4e lớp ngoài cùng tạo tối đa 4 liên kết cộng hóa tri Cacbon có thể có các số oxi hóa: - 4; 0; +2; +4 Các dạng thù hình: Dạng kim cương. Dạng than chì Fuleren gồm các phân tử Gcb Cto,... Fuleren Go có hình cẩu rỗng, có 32 mặt, 60 đỉnh là 60 nguyên tử cacbon. c có tính khử và tính oxi hóa ° 44 Tính khử: c + o2 ——■> CO2 co2 + c —í—> 2CO c + 4HNƠ3 (đ) -> co2f + 4NO2T + 2H2O Tínhoxihóa: c +2H2—to> CH4 ° to 4A1 + 3C —ĩ—» A14C3 Nhôm cacbua ★ BÀI TẬP: Tại sao hầu hết các hợp chất của cacbon lại là hợp chất cộng hóa trị? Tính oxi hóa cùa cacbon thể hiện ở phản ứng nào trong các phàn ứng sau? c + 02 > CO2 c + 2CuO > 2Cu + co2 c. 3C + 4A1 > AI4C3 D. c + H2O > CO + H2 Tính khử cùa cacbon thể hiện ờ phản ứng nào trong các phản ứng sau? A. 2C + Ca —> CaC2 B. c + 2H2 — —> CH4 c. c + co2 — —> 2CO D. 3C + 4A1 - > AI4C3 Lập phương trình hóa học của các phản ứng sau đây: t° H2SO4 (dặc) + c —-—> so2 + co2 + ? HNO3 (dặc) + c 10 > NO2 + CO2 + ? t° CaO + c —-—> CaC2 + co t° SiO2 + c —-—> Si + CO Đốt một mẫu than đá (chứa tạp chất không cháy) có khối lượng 0.600 kg trong oxi dư, thu được 1,06 m3 (đktc) khí cacbonic. Tính thành phần phần trăm khối lượng cúa cacbon trong mẫu than đá trên. HƯỚNG DẲN GIẢI: Hầu hết các hợp chất của cacbon là hợp chẩt cộng hóa trị vì c có 4 electron riêng lẻ ở lớp ngoài cùng tạo tối đa-4 liên kết cộng hóa trị T ính oxi hóa của c thể hiện ở trong phản ứng: 3C + 4A1 > AI4C3 Chọn c. Tính khử của c thể hiện phản ứng: c + co2 > 2CO Ơ!ỌM c. Phương trình hóa học 2H2SO4 (đ) + c —» 2SO2 + co2t + 2H2O 4HNO3 (đ) + c —> 4NO2 + CO2T + 2H2O. CaO + 3C - 200Q°C > CaC2 + co S1O2 + 2C —2CO + Si Phương trình phản ứng: c + o2 ■ t0 ) co2 12kg 22,4 m5 xkg 1,06 m3 x=l|12É = 0,5678(kg) 22,4 5 Thành phần phẩn trăm theo khối lượng của c là: 0,5678.100 _ '— = 94,64% 0,600