Giải bài tập Hóa 8 Bài 10: Hóa trị
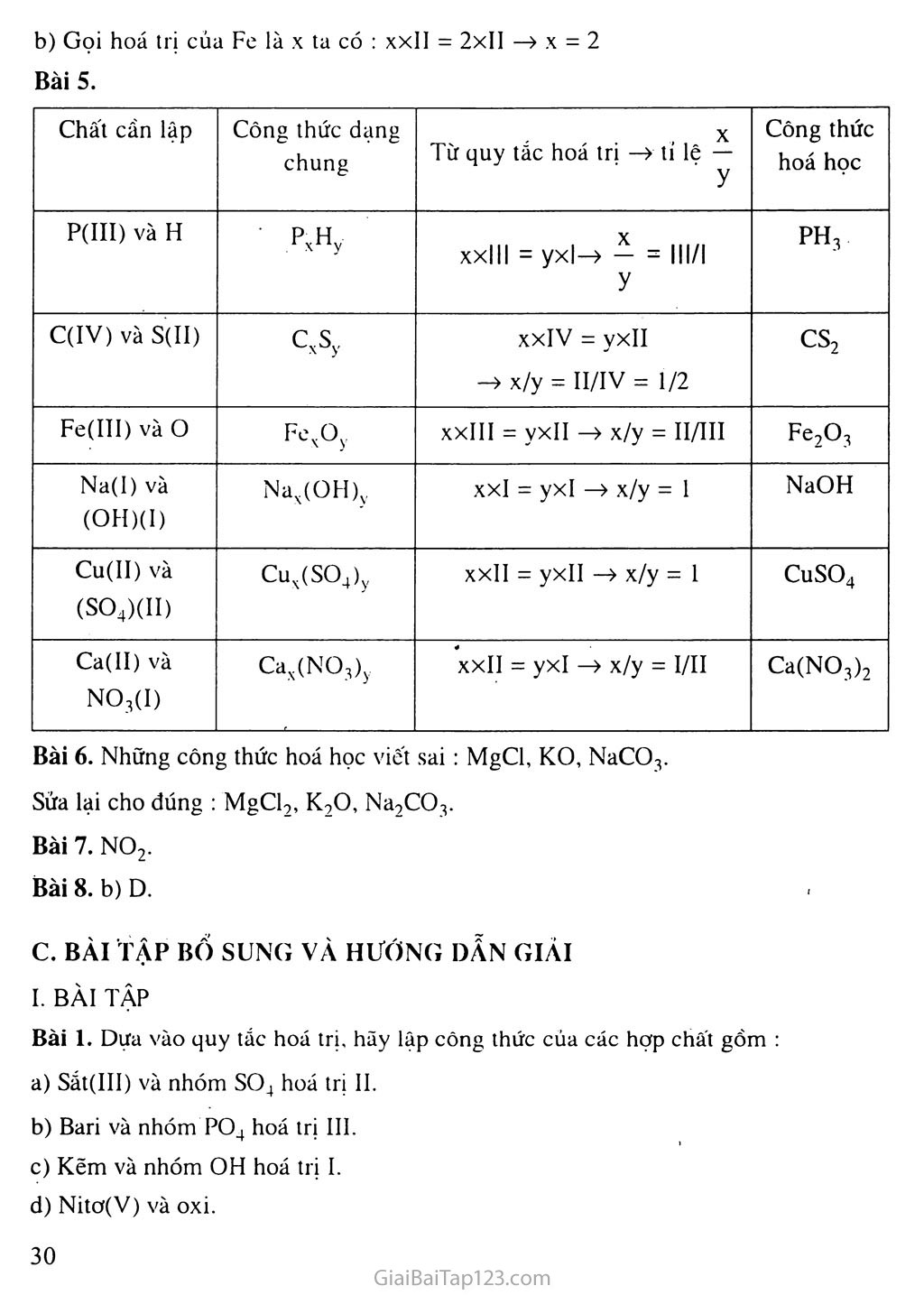
Bài 10. HOÁ TRỊ KIẾN THỨC TRỌNG TÂM Hoá trị biểu thị khả năng liên kết của nguyên tử nguyên tổ này với nguyên tử của nguyên tố khác hay nhóm nguyên tử khác. Khi xác định hoá trị, lấy hoá trị của nguyên tố H làm đơn vị, hoá trị của nguyên tố o bằng hai đơn vị. Quy tắc hoá trị : trong hợp chất hai nguyên tố AxBy thì : a.x= b.y (a, b là hoá trị tương ứng của hai nguyên tố A, B) (Quy tắc hoá trị đúng với cả khi A hay B là nhóm nguyên tứ) Tính được hoá trị cua nguyên tô' hoặc nhóm nguyên tử theo công thức hoá học cụ thể. Lập được công thức hoá học của hợp chất khi biết hoá trị của hai nguyên tố hoá học hoặc nguyên tố và nhóm nguyên tử tạo nên chất. HƯỚNG DẪN GIẢI BÀI TẬP TRONG SGK Bài 1. a) Hoá trị cúa nguyên tố (hay nhóm nguyên tử) là con số biểu thị khả năng liên kết của nguyên tử (hay nhóm.nguyên tử), được xác định theo hóa trị của H chọn làm đơn vị và hóa trị của o là hai đơn vị. b) Gọi hoá trị của Fe là X ta có : xxll = 2x11 —> X = 2 Bài 5. Chất cần lập Công thức dạng chung Từ quy tăc hoá tri —> ti lê — y Công thức hoá học P(III) và H ■ pxHý xxlll = yx|-> — = lll/l y ph3 C(IV) và S(II) cxsy xxiv = yxll -> x/y = II/IV = 1/2 CS2 Fe(IĨI) và o Fexoy xxIII = yxll —> x/y = II/III Fe2O3 Na(I) và (OH)(I) Nax(OH)y xxl = yxl —> x/y = 1 NaOH Cu(II) và (SO4)(II) Cux(so4)y XXII = yxll —> x/y = 1 CuSO4 Ca(II) và NO3(I) Cax(NO3)y xxll = yxl —> x/y = I/II Ca(NO3)2 Bài 6. Những công thức hoá học viết sai : MgCl, KO, NaCO3. Sửa lại cho đúng : MgClọ, KọO, Na9CO3. Bài 7. NO2. Bài 8. b) D. c. BÀI TẬP BỔ SUNG VÀ HƯỚNG DAN giải BÀI TẬP Bài 1. Dựa vào quy tắc hoá trị, hãy lập cõng thức cúa các hợp chất gồm : Sắt(III) và nhóm SO4 hoá trị II. Bari và nhóm PO, hoá tri III. ■ 1 Kẽm và nhóm OH hoá trị I. Nitơ(V) và oxi. Bài 2. Xác định hoá trị các nguyên tố và nhóm nguyên tử trong các hợp chất sau : Hoá trị của Fe trong Fe,O3; FeO : Fe3O4. Hoá trị cúa s trong H2S ; so2 ; SO3. Hoá trị của nhóm nguyên tử (SO4) trong H,SO4. Hoá trị cúa nhóm nguyên tứ (PO4) trong Mg3(PO4),. Bài 3. Tìm cống thức hoá học đúng ó' cột B ghép với cột A sao cho hợp lí. Cột A Cột B 1. Ca(II) với 0 a) A1,O3 2. Al(III) với 0 b) Ca,o, 3. C(IV) với 0 c)CO2 4. K(I) với 0 A13O, CaO K2O2 CO K2O Bài 4. Hãy đánh dấu X vào cột có chữ Đ nếu đúng và cột có chữ s nếu sai. Đ s a) Muối ăn : NaCl b) Axit clohidric : HC1 c) Cacbon đioxit : co d) Lưu huỳnh trioxit : so3 e) Lưu huỳnh đioxit : so, g) Đồng (I) oxit : CuO h) Sắt (III) oxit : Fe3O4 Bài 5. Trong một phân tứ của một oxit mangan có 2 nguyên tử Mn và 7 nguyên tử oxi. Vậy công thức của hợp chất oxit mangan đó là A. MnO. B. MnO2. c. Mn2O5. D. Mn2O7. Bài 6. Biết N có hoá trị IV, công thức hoá học phù hợp với quy tác hoá trị của nitơ là A. NO. B. N2O. c. N2O3. D. NO2. Bài 7. Biết hoá trị : Na(I), K(I), Mg(II), Al(III), P(V), CO3(II), SO4(II), PO4(III), OH (I). Chọn dãy có tất cá công thức hoá học viết đúng. NaCO3, K2SO4, A1(SO4)3. Na3PO4, A12O3, P2O5. c. MgNO3, FeCO3, Ca(CO3)2. D. A1(OH)2, NaOH. CuOH. Bài 8. Công thức hoá học cúa hợp chất của nguyên tố X với nguyên tố H và hợp chất của nguyên tố Y với nguyên tố C1 là : XH2, YClọ. Công thức hoá học thích hợp cho hợp chất của nguyên tố X và nguyên tố Y là A. XY3 B. XY c. X3Y2 D. y2x3 Bài 9. Hợp chất A1x(NO3)3 có phân tứ khối là 213. Giá trị của X là: A. 3. B. 2. c. 1. D.4. Bài 10. A12(SO4)3 là công thức hoá học của nhôm sunfat. Trong một phân tử nhôm sunfat có một nguyên tử Al, 1 nguyên tử s và 4 nguyên tử o. hai nguyên tử Al, 3 nguyên tử s và 4 nguyên tử o. c. hai nguyên tử Al, 3 nguyên tứ s và 12 nguyên tử o. D. 12 nguyên tử o, 3 nguyên tử s và 2 nguyên tử Al. Bài 11. Có 4 nguyên tắc sau : Hoá trị của nguyên tố là con số biểu thị khả năng liên kết của nguyên tứ nguyên tố đó với nguyên tử của nguyên tố khác. Trong các hợp chất, hiđro thường có hoá trị 1 và oxi thường có hoá trị II. Mỗi nguyên tố chí có một hoá trị. Một nguyên tố có thể có nhiều hoá trị. Thì nguyên tố X hoá trị III sẽ có công thức hoá học của muối sunfat là A. xso4 B. X(SO4)3 c. X2(SO4)3 D. X3SO4 Bài 12. Một hợp chất thành phần có 70% Fe về khối lượng, còn lại là oxi. Hoá trị của Fe trong hợp chất là A. I. B. II. c. III. D. IV. II. HƯỚNG DẪN GIẢI Bài 1. Các công thức cần'lập là Fe2(SO4)3 ; b) Ba3(PO4)2 ; c) Zn(OH)2 ; d) N205 Bài 2. a) Fe2O3 : Fe có hoá.trị III. FcO : Fe có hoá trị II. Fe3O4(Fe2O3 . FcO) : Fe có hoá trị II và III. H2S : s có hoá trị II. so, : s có hoá trị IV. so3 : s có hoá trị VI. H2SO4 : Nhóm nguyên tử (SO4) có hoá trị II. Mg3(PO4)2 : nhóm nguyên tứ (PO4) có hoá trị III. Bài 3. 1 ghép với e ; 2 ghép với a ; 3 ghép với c ; 4 ghép với i. Bài 4. Đ s a) Muối ăn : NaCl X b) Axit clohiđric : HC1 X c) Cacbon đioxit : co X d) Lưu huỳnh trioxit : so. X e) Lưu huỳnh đioxit : so. X g) Đồng (I) oxit : CuO X h) Sắt (III) oxit : Fe,O4 X Bài 5. D Bài 6. D Bài 7. B Bài 8. B Bài 9. c Bài 10. c Bài 11. c Bài 12. c.