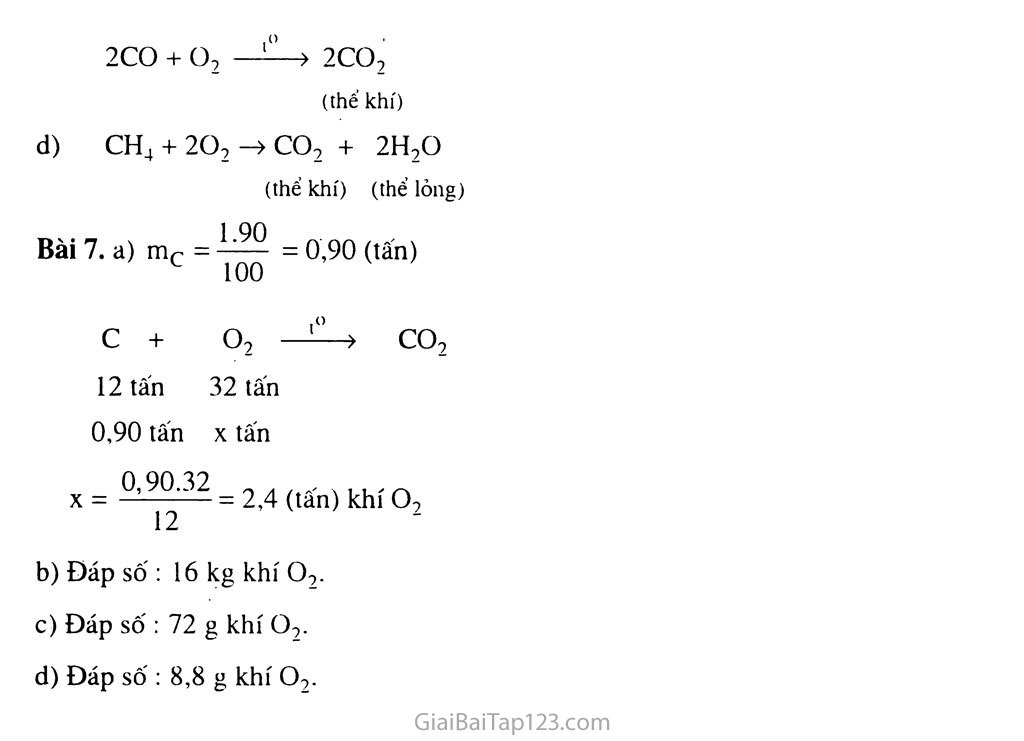Giải bài tập Hóa 8 Bài 25: Sự oxi hóa - Phản ứng hóa hợp - Ứng dụng của oxi
Bài 25. Sự OXI HOÁ - PHẢN ỨNG HOÁ HỢP. ■ ■ ỨNG DỤNG CỦA OXI A. KIẾN THỨC TRỌNG TÂM Sự oxi hoá là sự tác dụng của oxi với một chất khác. Khái niệm phản ứng hoá hợp. ứng dụng của oxi trong đời sống và sản xuất. Xác định được có sự oxi hoá trong một số hiện tượng thực tế. Nhận biết được một số phản ứng hoá học cụ thể thuộc loại phản ứng hoá hợp. B. HƯỚNG DẪN GIẢI BÀI TẬP TRONG SGK Bài 1. a) Sự tác dụng của oxi với một chất là sựoxi hoá. Phản ứng hoá hợp là phản ứng hoá học trong đó chỉ có một chất mới được tạo thành từ hai hay nhiều chất han dần. Khí oxi cấn cho sự hô hấp cúa người, động vật và cần để đốt nhiên liệu trong đời sống và sán xuất. Bài 3. CH4 + 2O2 ——> CO2 + 2H2O 22,4 dm3 2.22,4 dm3 Lượng khí metan nguyên chất : 1000 dm3 - 20 dm3 = 980 (dm3). Thể tích khí oxi (đktc) cần dùng : "•—2,4.980 _ 1960 (dm3). 22,4 Bài 4. a) Khi cho một cây nến đang cháy vào một lọ thuỷ tinh và đậy nút kín, ngọn lửa cây nến sẽ yếu dần rồi tắt. Đó là vì khi nến cháy, lượng oxi trong không khí sẽ bị giảm dần rồi hết, lúc đó nến sẽ bị tắt. Bài 5. a) Khi càng lên cao, tỉ lộ lượng khí oxi trong không khí càng giảm là vì khí oxi nặng hơn không khí. b) Phản ứng cháy cúa các chất trong bình chứa khí oxi mãnh liệt hơn trong không khí là vì ớ trong'khí oxi, bề mật tiếp xúc của chất cháy với oxi lớn hơn nhiều lần ở trong không khí (thể tích cúa khí oxi chi chiếm có 1/5, còn nitơ chiếm tới 4/5), ngoài ra một phần nhiệt còn bị tiêu hao do đốt nóng khí nitơ. c. BÀI TẬP BỔ SUNG VÀ HƯỚNG DAN giải I. BÀI TẬP Bài 1. Phát biểu nào sau đây là sai ? Oxi là chất khí không màu. không mùi, không vị. Oxi nặng hơn không khí và ít tan trong nước, c. Oxi tác .dụng với kim loại không tạo ra oxit. D. Sự oxi hoá toả nhiệt mà không phát sáng. Bài 2. Nhận định nào dưới đây là đúng ? A. Sự tác dụng của oxi với một chất không được gọi là sự oxi hoá. B. Phản ứng hoá hợp là phản ứng hoá học trong đó chỉ có một chất mới được tạo thành từ hai hay nhiều chất ban đầu. c. Càng lên cao thì tỉ lệ thể tích khí oxi trong không khí càng tăng. D. Sự quang hợp của cây xanh làm giảm lượng oxi trong không khí. Bài 3. Có những phản ứng sau : 4Na + O2 —> 2Na2O HC1 +NaOH -> NaCl + H2O c) 4P + 5O2 ' 2P2O5 d) 1° c + 02 1 -> co2 e) CH4 + 2O-) - co2 + 2H2O f) CaCO3 l° -» CaO + co2 Phản ứng hoá hợp gồm những phản ứng : A. c, d, e. B. b, e, f. c. a, c, d. D. a, c, e. Bài 4. Dùng 2 mol khí oxi có thể để đốt cháy vừa hết A. 54 gam Al. B. 31gamP. c. 32 gam s. D. 24 gam c. Bài 5. Đốt cháy bột than trong bình chứa 4,48 lít khí oxi (đktc). Sau phản ứng người ta thu được 6,6 gam khí co2. Tính khối lượng than đã tham gia phản ứng. Tính thể tích khí oxi còn dư sau phản ứng. Bài 6. Cho một số chất sau : cacbon, hiđro, magie, metan, cacbon oxit. Hãy cho biết sự oxi hoá nào sẽ tạo ra oxit ở thể rắn ? oxit ở thể lỏng ? oxit ở thể khí ? oxit ở thể khí và oxit ở thể lỏng ? Viết các phương trình hoá học xảy ra ? Bài 7. Tính khối lượng khí oxi cần dùng đê đốt cháy hoàn toàn : Một tấn than chứa 90% cacbon. Những tạp chất còn lại không cháy được. 4 kg khí metan (CH4). Hỗn hợp có 8 g khí hiđro và 2 g khí metan. Hỗn hợp có 0,15 mol c và 0,125 mol s. II. HƯỚNG DẪN GIẢI Bài 1. c Bài 2. B Bài 3. c Bài 4. D Bài 5. n(b = V, o2 _ 4,48 22,4 22,4 = 0,2 (mol). Ta có phương trình : c + 02 -» co2 Ban đầu : X 0,2 Phản ứng : 0,15 0,15 0,15 Sau phản ứng 0,05 0,15 lco2 co2 M co2 a) Theo phương trình hoá học : nc cháy = 0,15 => mCch.-iỵ =nc.Mc =0,15. 12= l,8(gam). —— = 0,15 (mol). 44 b) noxi dư = °’05 (m°D- =5 moxidư = 0,05.32 =1,6 (gam). Bài 6. a) 2Mg + 02 —2MgO (thể rán) 2H2 + o2 —2H2O (thể lỏng) c + 02 —co2 (thế khí) 2C0 + o2 —2C0, (thế khí) d) CH4 + 2O2 -> co2 + 2H2O (thể khí) (thể lỏng) 1.90 . Bài 7. a) mr = —= 0,90 (tấn) c 100 c + o2 —co2 12 tấn 32 tấn 0,90 tấn X tấn 0,90.32 - , , . . ,, , „ X = ——— = 2,4 (tấn) khí O, 12 Đáp số : 16 kg khí 02. Đáp số : 72 g khí 02. Đáp số : 8,8 g khí Oọ.