SGK Hóa Học 10 - §1. Sự xen phủ các obitan nguyên tử. Sự lai hóa các obitan nguyên tử
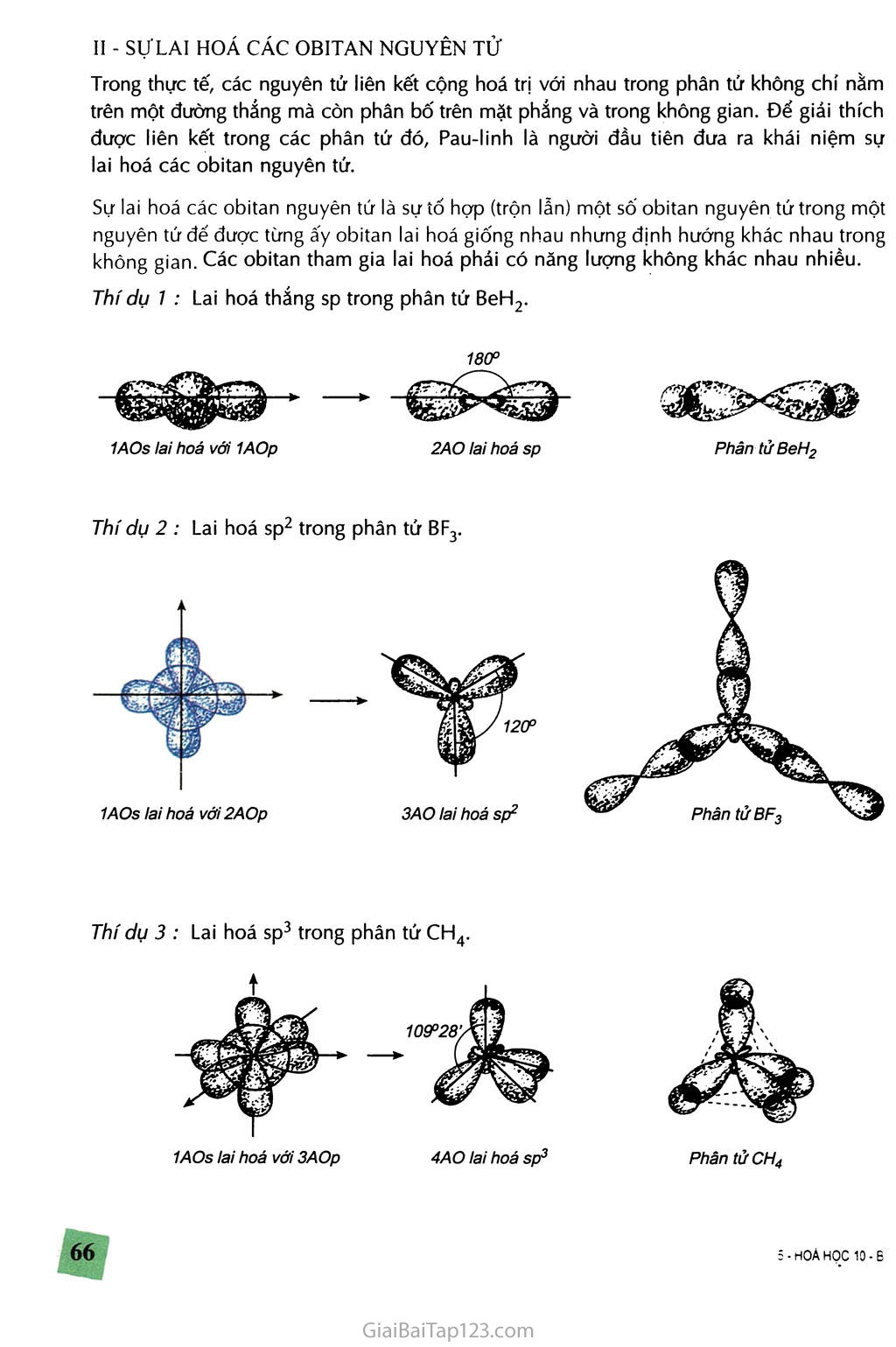
Bài đọc thêm § 1. Sự XEN PHỦ CÁC OBITAN NGUYÊN TỬ Sự LAI HOÁ CÁC OBIT AN NGUYÊN TỬ I ’ SỰXEN PHỦ CÁC OBITAN NGUYÊN TỬ Theo quan điểm hiện đại, khi 2 nguyên tứ lại gần nhau, nếu xác suất tìm thấy electron ớ giữa 2 nguyên tứ đó tăng lên thì có liên kết hoá học, nếu nó bằng không thì không có liên kết hoá học. Đế giái thích sự tạo thành liên kết hoá học nói trên, người ta đưa ra khái niệm sự xen phú các obitan nguyên tứ. Có hai kiếu xen phú : -Xen phú trục : Sự xen phú xáy ra trên trục nối giữa hai hạt nhân nguyên tứ. Sự xen phủ này tạo ra liên kết ơ (xích ma). Thí dụ : Sự xen phú trục giữa 2 obitan s cúa 2 nguyên tứ hiđro tạo liên kết ơ trong phân tứ H2. 1s 1s Sự Xen phủ của 2 obitan 1s của hai nguyên tử hiđro - Xen phú bén : Sự xen phú thực hiện ớ hai bên trục nối giữa hai hạt nhân nguyên tứ. Sự xen phú này tạo ra liên kết 71 (pi). Thí dụ : Xen phú bên trong phân tứ C2H4. Sự xen phú trục giữa hai nguyên tứ lớn hơn xen phú bên nên liên kết ơ bền hơn liên kết 7t. II - SựLAI HOÁ CÁC OBITAN NGUYÊN TỬ Trong thực tế, các nguyên tử liên kết cộng hoá trị với nhau trong phân tử không chí nằm trên một đường thẳng mà còn phân bố trên mặt phẳng và trong không gian. Để giải thích được liên kết trong các phân tứ đó, Pau-linh là người đầu tiên đưa ra khái niệm sự lai hoá các obitan nguyên tứ. Sự lai hoá các obitan nguyên tử là sự tổ họp (trộn lẫn) một số obitan nguyên tử trong một nguyên tứ để được từng ấy obitan lai hoá giống nhau nhưng định hướng khác nhau trong không gian. Các obitan tham gia lai hoá phải có năng lượng không khác nhau nhiều. Thí dụ 7 : Lai hoá thắng sp trong phân tứ BeH2. 180° 1AOs lai hoá với 1AOp 2AO lai hoá sp Phân tử BeH2 Thí dụ 2 : Lai hoá sp2 trong phân tứ BF3. 1AOs lai hoá với 3AOp 4AO lai hoá sp3 Phân tử CH4 Việc chọn dạng lai hoá nào đế giái thích sự liên kết trong phân tứ tuỳ thuộc vào cấu trúc Thí dụ, phân tứ metan CH4 có cấu trúc tứ diện, ta chọn 4 AO lai hoá sp3 cúa nguyên tứ cacbon đế giái thích sự xen phú trục cúa chúng với 4AOs cúa 4 nguyên tứ H tạo ra 4 liên kết ơ trong phân tứ metan với góc liên kết 109°28. Còn trong phân tứ BeF3 có cấu trúc tam giác đều, ta lại phái chựn lai hoá sp2 đế giái thích góc liên kết trong phân tứ đó là 120° ... Obitan lai hoá chí xen phú trục để tạo liên kết ơ. . •