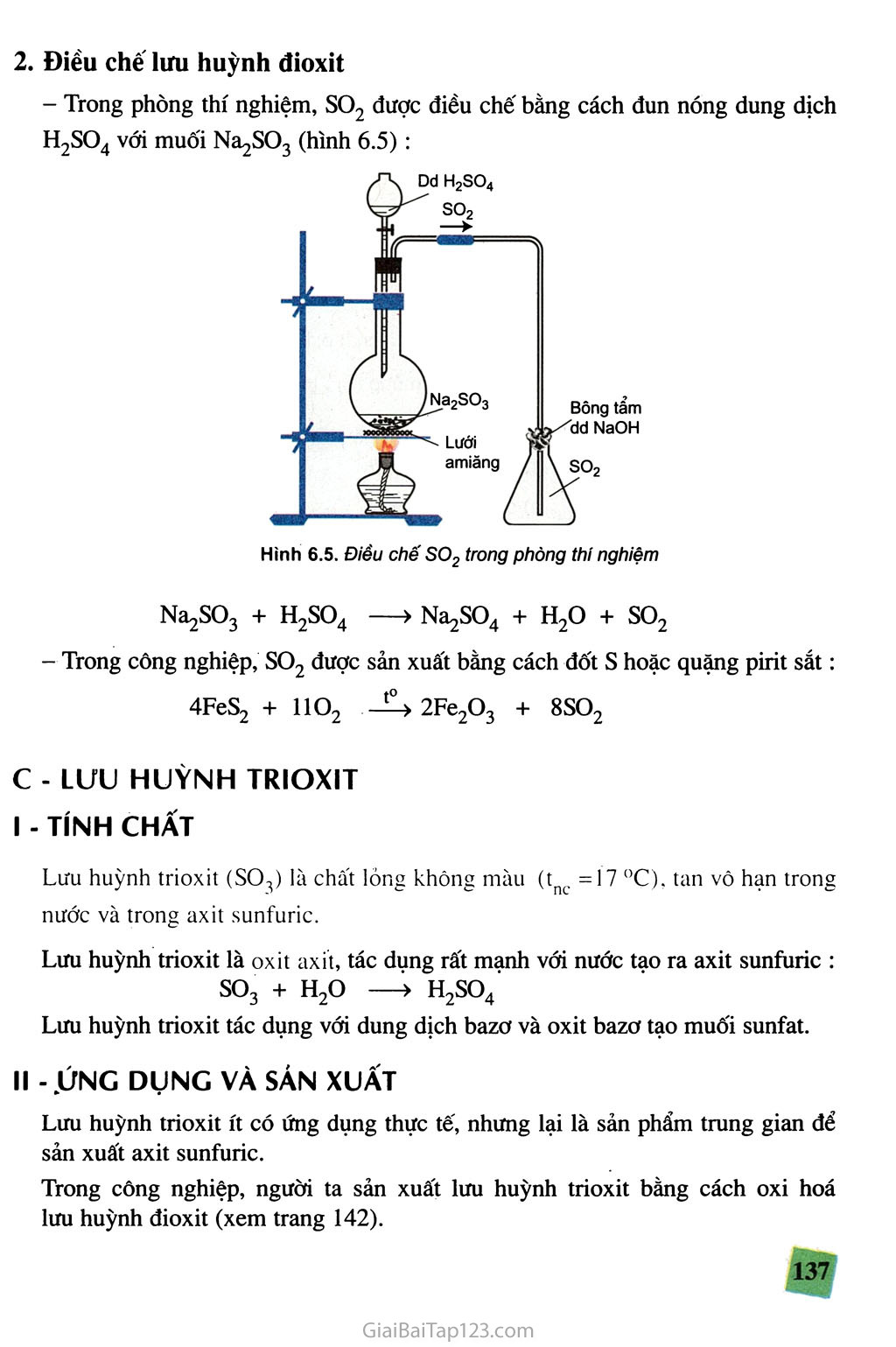
SGK Hóa Học 10 - Bài 32. Hiđro sunfua - Lưu huỳnh đioxit - Lưu huỳnh trioxit
HIĐRO SUNFUA LƯU HUỲNH ĐIOXIT LUU HUỲNH TRIOXIT • Hiđro sunfua, lưu huỳnh đioxit và lưu huỳnh trioxit có những tính chất nào giống nhau và khác nhau ? Vì sao ? Những phản ứng hoá học nào có thế chứng minh cho những tính chất này ? A - HIĐRO SUNFUA - TÍNH CHẤT VẬT LÍ Hiđro sunfua (H9S) là chất khí, không màu, mùi trứng thối và rất độc. Chỉ 0,1% H2S có trong không khí đã gây nhiễm độc mạnh. Khí H2S hoi nặng hơn không khí = — -1,17^, hoá lỏng ở nhiệt độ - 60 °C, tan ít trong nước (ở 20 °C và 1 atm, khí H2S có độ tan là 0,38 g trong 100 g nước). - TÍNH CHẤT HOÁ HỌC Tính axit yếu Hiđro sunfua tan trong nước tạo thành dung dịch axit rất yếu (yếu hơn axit cac- bonic), có tên là axit sunfuhidric (H2S). Axit sunfuhidric tác dụng với dung dịch bazơ như NaOH, tạo nên 2 loại muối: muối trung hoà như NajS chứa ion s2_ và muối axit như NaHS chứa ion HS_. Tính khử mạnh Trong hợp chất H2S, nguyên tố lưu huỳnh có số oxi hoá thấp nhất là -2. Khi tham gia phản ứng hoá học, tuỳ thuộc vào điều kiện của phản ứng -2 mà nguyên tố lưu huỳnh có số oxi hoá -2 ( s ) có thể bị oxi hoá thành lưu 0 +4 huỳnh tự do (s ), hoặc lưu huỳnh có số oxi hoá +4 ( s ), hoặc lưu huỳnh có số +6 oxi hoá +6 ( s ). Người ta nói, hiđro sunfua có tính khử mạnh (dễ bị oxi hoá). Những phản ứng hoá học chứng minh tính khử của hiđro sunfua : Trong những điều kiện bình thường, dung dịch H9S tiếp xúc với oxi của không khí, dần trở nên 0 vẩn đục màu vàng do Họs bị oxi hoá thành s : -20 -20 2H2S + 02 —> 2H2O + 2S Khi đốt khí H2S trong không khí, khí H2S cháy với ngọn lửa màu xanh nhạt ; H2S bị oxi hoá thành SO2 : -2 __ t0 +4 2H2S + 3O2 -4-4 2H2O + 2SO2 Nếu đốt cháy khí H?s ở nhiệt độ không cao hoặc thiếu oxi, khí H?s bị oxi hoá thành lưu huỳnh tự do, màu vàng (hình 6.4). Ill - TRẠNG THÁI Tự NHIÊN VÀ ĐIỀU CHÊ Trong tự nhiên, hiđro sunfua có trong một số nước suối, trong khí núi lửa và bốc ra từ xác chết của người và động vật... Trong công nghiệp, người ta không sản xuất khí hiđro sunfua. Trong phòng thí nghiệm, người ta điều chế bằng phản ứng hoá học của dung dịch axit clohiđric với sắt(II) sunfua : FeS + 2HC1 > FeCl2 + H2sf B - LƯU HUỲNH ĐIOXIT I - TÍNH CHẤT VẬT LÍ Lưu huỳnh đioxit (SOỌ) (khí suníurơ) là chất khí không màu, mùi hắc, nặng hơn không khí ^.d = ~ 2,2^), hoá lỏng ở -10 °C, tan nhiều trong nước (ở 20 °C, 1 thể tích nước hoà tan được 40 thể tích khí SO2). Lưu huỳnh đioxit là khí độc, hít thở phải không khí có khí này sẽ gây viêm đường hô hấp. - TÍNH CHẤT HOÁ HỌC Lưu huỳnh đỉoxit là oxit axit SO2 tan trong nước tạo thành dung dịch axit suníurơ H2SO3 : so2 + H2O H2SO3 Axit suníurơ là axit yếu (mạnh hơn axit sunfuhidric và axit cacbonic) và không bền, ngay trong dung dịch H2SO3 cũng bị phân huỷ thành SO2 và H2O. SO2 tác dụng với dung dịch bazơ như NaOH, tạo nên 2 loại muối : Muối trung hoà như Na2SO3 (chứa ion sunfit soj- ) và muối axit như NaHSO3, (chứa ion hidrosunfit HSO3). Lưu huỳnh đỉoxỉt là chất khử và là chất oxi hoá Lưu huỳnh đioxit là chất khử Khi dẫn khí SO2 vào dung dịch brom có màu vàng nâu nhạt, dung dịch brom bị mất màu : +4 0 -1 +6 so2 + Br2 + 2H2O > 2HBr + H2SO4 SOọ đã khử Br2 có màu thành HBr không màu. Lưu huỳnh đioxit là chất oxì hoá Khi dẫn khí SO2 vào dung dịch axit sunfuhidric Họs, dung dịch bị vẩn đục màu vàng : +4 -2 0 so2 + 2H2S —> 3SÌ + 2H2O SOọ đã oxi hoá HỌS thành s. - ỨNG DỤNG VÀ ĐIỀU CHÊ LƯU HUỲNH ĐIOXIT ứng dụng Lưu huỳnh đioxit được dùng để sản xuất H9SO4 trong công nghiệp, làm chất tẩy trắng giấy và bột giấy, chất chống nấm mốc lương thực, thực phẩm ... Điều chê lưu huỳnh đioxỉt - Trong phòng thí nghiệm, SO9 được điều chế bằng cách đun nóng dung dịch H2SO4 với muối Na2SO3 (hình 6.5) : Hình 6.5. Điều chế SO2 trong phòng thí nghiệm Na2SO3 + H2SO4 —> Na^c^ + H2O + SO2 — Trong công nghiệp, SO2 được sản xuất bằng cách đốt s hoặc quặng pirit sắt: 4FeSọ + 1102 —> 2Fe2O3 + 8SO2 c - LƯU HUỲNH TRIOXIT - TÍNH CHẤT Lưu huỳnh trioxit (SO3) là chất lỏng không màu (tnc =17 °C), tan vô hạn trong nước và trong axit sunfuric. Lưu huỳnh trioxit là oxit axit, tác dụng rất mạnh với nước tạo ra axit sunfuric : so3 + H2O —> H2SO4 Lưu huỳnh trioxit tác dụng với dung dịch bazơ và oxit bazơ tạo muối sunfat. - .ÚNG DỤNG VÀ SÁN XUẤT Lưu huỳnh trioxit ít có ứng dụng thực tế, nhưng lại là sản phẩm trung gian đổ sản xuất axit sunfuric. Trong công nghiệp, người ta sản xuất lưu huỳnh trioxit bằng cách oxi hoá lưu huỳnh đioxit (xem trang 142). BÀI TẬP Lưu huỳnh đioxit có thể tham gia những phản ứng sau : so2 + Br2 + 2H2O > 2HBr + H2SO4 (1) so2 + 2H2S > 3S + 2H2O (2) Câu nào sau đây diễn tả không đúng tính chất của các chất trong những phản ứng trên ? Phản ứng (1) : so2 là chất khử, Br2 là chất oxi hoá. Phản ứng (2): so2 là chất oxi hoá, H2S là chất khử. c. Phản ứng (2): so2 vừa là chất khử, vừa là chất oxi hoá. D. Phản ứng (1) : Br2 là chất oxi hoá, phản ứng (2) : H2S là chất khử. Hãy ghép cặp chất và tinh chất của chất sao cho phù hợp : Các chất Tính chất của chất A. s a) có tính oxi hoá B. so2 b) có tính khử c. H2S c) có tính oxi hoá và tính khử D. H2SO4 chất khí, có tính oxi hoá và tính khử không có tính oxi hoá và cũng không có tính khử Cho phản ứng hoá học : H2S + 4CI2 + 4H2O > H2SO4 + 8HCI Câu nào sau đây diễn tả đúng tính chất các chất phản ứng ? H2S là chất oxi hoá, Cl2 là chất khử. H2S là chất khử, H2O là chất oxi hoá. c. Cl2 là chất oxi hoá, H2O là chất khử. D. Cl2 là chất oxi hoá, H2S là chất khử. Hãy cho biết những tính chất hoá học đặc trưng của hiđro sunfua. lưu huỳnh đioxit. Dẩn ra những phản ứng hoá học để minh hoạ. Dần khí so2 vào dung dịch KMnO4 màu tím, nhận thấy dung dịch bị mất màu vì xảy ra phản ứng hoá học sau : so2 + KMnO4 + H2O > K2SO4 + MnSO4 + H2SO4 Hãy cân bằng phương trình hoá học trên bằng phương pháp thăng bằng electron. Hãy cho biết vai trò của so2 và KMnO4 trong phản ứng trên. a) Bằng phản ứng hoá học nào có thể chuyển hoá lưu huỳnh thành lưu huỳnh đioxit và ngược lại lưu huỳnh đioxit thành lưu huỳnh ? b) Khí lưu huỳnh đioxit là một trong những khí chủ yếu gây mưa axit. Mưa axit phá huỷ những công trình được xây dựng bằng đá, thép. Tính chất nào của khí so2 đã huỷ hoại những công trình này ? Hãy dẫn ra phản ứng hoá học để chứng minh. Hãy dẫn ra những phản ứng hoá học để chứng minh rằng lưu huỳnh đioxit và lưu huỳnh trioxit là những oxit axit. * . Cho hỗn hợp gồm Fe và FeS tác dụng với dung dịch HCI (dư), thu được 2,464 lít hỗn hợp khí (đktc). Cho hỗn hợp khí này đi qua dung dịch Pb(NO3)2 (dư), thu được 23,9 g kết tủa màu đen. Viết phương trình hoá học của các phản ứng đã xảy ra. Hỗn hợp khí thu được gồm những khí nào ? Thể tích mỗi khí là bao nhiêu (đktc) ? Tính khối lượng của Fe và FeS có trong hỗn hợp ban đầu. Đốt cháy hoàn toàn 2,04 g hợp chất A, thu được 1,08 g H2O và 1,344 l SO2 (đktc). Hãy xác định công thức phân tử của hợp chất A. Dẩn toàn bộ lượng hợp chất A nói trên đi qua dung dịch axit sunfuric đặc thấy có kết tủa màu vàng xuất hiện. Hãy giải thích hiện tượng và viết phương trình hoá học của phản ứng xảy ra. Tính khối lượng chất kết tủa thu được. Hấp thụ hoàn toàn 12,8 g so2 vào 250 ml dung dịch NaOH 1M. Viết phương trình hoá học của các phản ứng có thể xảy ra. Tính khối lượng muối tạo thành sau phản ứng.